
把一小块金属钠投入100 mL 0.15 mol/LCuCl2溶液中,收集到产生的气体的体积为1.456L(标准状况下),此时溶液体积仍然为100 mL 。计算
(1)加入金属钠的质量
(2)反应后溶液的pH
⑴ 2.99 g ⑵ 14
【解析】
试题分析:(1)生成的氢气体积是1.456L(标准状况下)
则氢气的物质的量是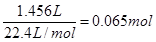
所以根据反应式2Na+2H2O=2NaOH+H2可知
加入的计算钠的质量是0.065mol×2×23g/mol=2.99g
(2)生成的氢氧化钠的物质的量是0.13mol
其中和氯化铜反应的氢氧化钠是0.1L×0.15mol/L×2=0.03mol
所以剩余氢氧化钠的物质的量是0.13mol-0.03mol=0.1mol
则氢氧化钠溶液的浓度是0.1mol÷0.1L=1mol/L
因此氢离子的浓度是10-14mol/L
所以pH=14
考点:考查根据化学方程式进行的有关计算,以及pH的计算等
点评:本题是基础性试题的考查,难度不大。主要是训练学生的规范答题能力,有利于培养学生的学习习惯,提高学习效率。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:0101 期末题 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2008-2009学年北京101中高一(上)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com