
| A�� | �����ɳ����ﵽ�����ʱ������NaOH��Һ�����Ϊ150mL | |
| B�� | ������ȫ���ܽ�ʱ�ռ���NO��������Ϊ0.336L����״���£� | |
| C�� | ������ȫ���ܽ�ʱ���μӷ�Ӧ����������ʵ���һ����0.6mol | |
| D�� | �μӷ�Ӧ�Ľ�����������һ����9.9g |
���� ��һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O��
��Ӧ�����Һ�м��������3mol/L NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������7.65g����������þ��������ͭ����������������Ϊ7.65g�������������ʵ���Ϊ$\frac{7.65g}{17g/mol}$=0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
A�������ɵij����ﵽ�����ʱ����Һ������ΪNaNO3��������غ��֪n��NaNO3��=2n������ͭ+����þ�������������غ���n��NaOH��=n��NaNO3�����ٸ���V=$\frac{n}{V}$���㣻
B�����ݵ���ת���غ����NO���ʵ�����������岻һ���DZ�״���жϣ�
C�����ݵ�Ԫ���غ�n��HNO3��=2n������ͭ+����þ��+n��NO����
D������þ��ͭ���ܵ����ʵ����Լ�������������������ĺ����й������㣮
��� �⣺��һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O��
��Ӧ�����Һ�м��������3mol/L NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������7.65g����������þ��������ͭ����������������Ϊ7.65g�������������ʵ���Ϊ$\frac{7.65g}{17g/mol}$=0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
A�������ɵij����ﵽ�����ʱ����Һ������ΪNaNO3��������غ��֪n��NaNO3��=2n������ͭ+����þ��=0.225mol��2=0.45mol�����������غ���n��NaOH��=n��NaNO3��=0.45mol���ʴ�ʱ����������Һ�����Ϊ$\frac{0.45mol}{3mol/L}$=0.15L=150mL����A��ȷ��
B�����ݵ���ת���غ��֪���ɵ�NO���ʵ���Ϊ$\frac{0.225mol��2}{3}$=0.15mol����״���£�����NO�����Ϊ0.15mol��22.4L/mol=3.36L����B����
C�����ݵ�Ԫ���غ�n��HNO3��=2n������ͭ+����þ��+n��NO��=0.225mol��2+0.15mol=0.6mol����C��ȷ��
D��þ��ͭ���ܵ����ʵ���Ϊ0.225mol���ٶ�ȫΪþ������Ϊ0.225mol��24g/mol=5.4g����ȫΪͭ������Ϊ0.225mol��64g/mol=14.4g�����Բμӷ�Ӧ�Ľ�������������m��Ϊ5.4g��m��14.4g����D����
��ѡAC��
���� ������Ҫ���������йؼ��㣬�漰þͭ�����ᷴӦ�����ɵ������������Ʒ�Ӧ���ۺϿ���ѧ���ĵ�ʧ�����غ㡢�����غ���ۺ����úͽ�������������������һ�����������ĺ��⣬�ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��N2��CCl4 | B�� | CH4��NH3��H2O | C�� | CO2��CS2��Cl2 | D�� | HCl��NO��Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��F
��F
 +O2$��_{��}^{Cu}$2
+O2$��_{��}^{Cu}$2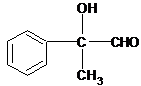 +2H2O
+2H2O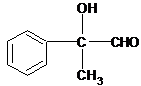 +2Cu��OH��2$\stackrel{��}{��}$
+2Cu��OH��2$\stackrel{��}{��}$ +Cu2O��+2H2O
+Cu2O��+2H2O ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ԫ����ԭ�������ĵ���ԭ�Ӱ뾶��С | |
| B�� | �����Ԫ����ԭ�������ĵ����������������� | |
| C�� | �����Ԫ�صĵ�����������ȼ�����ɹ������� | |
| D�� | �����Ԫ����ԭ�������ĵ�������������Ӧ��ˮ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3��g��+HCl��g����NH4Cl��s�����÷�Ӧ���Է����У�����ֵ���� | |
| B�� | SO2��g����S��s��+O2��g����H��0����S��0����÷�Ӧ���Է����� | |
| C�� | O2��g��+2H2��g���T2H2O��l����H��0�����º�ѹ��һ�����Է����� | |
| D�� | ij�¶���2SO2��g��+O2��g���T2SO3��g����K1=400������ͬ�¶���2SO3��g��?2SO2��g��+O2��g����ƽ�ⳣ��Ϊ$\frac{1}{400}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | P3=P4��y���ʾC��������� | |
| B�� | P3��P4��y���ʾB���������� | |
| C�� | P3��P4��y���ʾ���������ܶ� | |
| D�� | P3��P4��y���ʾ��������ƽ��Ħ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com