
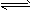 2NH3(g),分别在不同时测定NH3的含量,然后绘制出下图
2NH3(g),分别在不同时测定NH3的含量,然后绘制出下图
科目:高中化学 来源: 题型:
研究和开发CO2 和CO的创新利用是环境保护和资源利用
的双赢的课题。
I.CO可用于合成甲醇。在压强为0.1Mpa条件下,在体积为bL的密
闭容器中充入amolCO和2amolH2,在催化剂作用下合成甲醇;
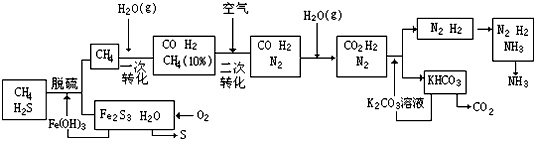
![]() 平衡时CO的转化率与温度,压强的关系如下图:
平衡时CO的转化率与温度,压强的关系如下图:
 (1)100℃时,该反应的平衡常数:
(1)100℃时,该反应的平衡常数:
K= ;(用a、b的代数式表
示)。若一个可逆反应的平衡常数K值
很 大,对此反应的说法正确的是:
(填序号)
A.该反应使用催化剂意义不大;
B.该反应发生将在很短时间内完成;
C. 该反应达到平衡时至少有一种反应物
百分含量很小;
D.反应物的转化率一定高:
(2)在温度和容积不变的情况下,再向平衡体系中充入amolCO,2amolH2,达到平衡时
CO转化率 (填“增大”,“不变”或“减小”,下同)平衡常数: 。
(3)在某温度下,向一容积不变的密闭容器中充入2.5molCO,7.5molH2,反应生成CH3OH
(g),达到平衡时,CO转化率为90%,此时容器内压强为开始时的压强 倍。
11.某温度条件下,若将CO2(g)和H2(g)以体积比1:4混合,在适当压强和催化剂
作用下可制得甲烷,己知:
![]()
则![]() 和
和![]() 反应生成液态水的热化学方程式为:
反应生成液态水的热化学方程式为:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com