
【题目】工业上可由氢气、氮气合成氨气,溶于水形成氨水。一定温度下,向2L固定体积的密闭容器中加入N2(g)和H2(g),发生反应:N2(g)+3H2(g)![]() 2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
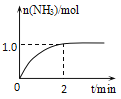
(1)0~2min内的平均反应速率v(H2)=___。
(2)该温度下,反应的平衡常数表达式K=___。
其平衡常数K与温度T的关系如下表:
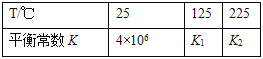
试判断K1___K2(填写“>”、“=”或“<”)。
(3)能说明该合成氨反应已达到平衡状态的是___(选填编号)。
a.3v(N2)=v(H2)
b.容器内压强保持不变
c.混合气体的密度保持不变
d.25℃时,测得容器中c(NH3)=0.2mol·L-1,c(H2)=c(N2)=0.01mol·L-1
常温下,某同学将盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如表。
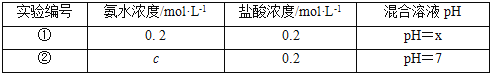
请回答:
(4)①中所得混合溶液,pH___7(填“>”、“<”或“=”);②中c__0.2(填“>”、“<”或“=”),所得混合溶液中各离子浓度大小关系为___。
(5)请你设计一个能证明一水合氨是弱电解质的简要方案___。
【答案】0.375mol/(L·min) ![]() > bd < > c(Cl-)=c(NH4+)>c(H+)=c(OH-) 用玻璃棒蘸取0.1mol·L-1NH4Cl溶液滴在pH试纸上,显色后跟标准比色卡比较,测出pH,pH<7
> bd < > c(Cl-)=c(NH4+)>c(H+)=c(OH-) 用玻璃棒蘸取0.1mol·L-1NH4Cl溶液滴在pH试纸上,显色后跟标准比色卡比较,测出pH,pH<7
【解析】
(1)由图像可知,生成氨气的物质的量为1mol,则消耗氢气的物质的量为1.5mol,反应速率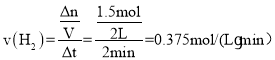 ,故答案为:0.375mol/(L·min);
,故答案为:0.375mol/(L·min);
(2)结合方程式,反应的平衡常数表达式K=![]() ,反应为放热反应,升高温度平衡逆向移动,平衡常数减小,则K1>K2,故答案为:
,反应为放热反应,升高温度平衡逆向移动,平衡常数减小,则K1>K2,故答案为:![]() ;>;
;>;
(3)a.根据方程式系数与反应速率的关系,任何状态下,都有3v(N2)=v(H2),则3v(N2)=v(H2)不能说明反应到达平衡状态,故a错误;
b.从方程式可知,该反应是气体的总物质的量是可变的量,当容器内压强保持不变,则气体的总物质的量不变,说明该反应达到平衡状态,故b正确;
c.根据质量守恒定律,气体的总质量始终保持不变,而该反应在恒容条件下进行,则混合气体的密度始终保持不变,故c错误;
d.25℃时,测得容器中c(NH3)=0.2mol·L-1,c(H2)=c(N2)=0.01mol·L-1,计算浓度熵![]() ,则反应处于平衡状态,故d正确;
,则反应处于平衡状态,故d正确;
综上所述,故答案为:bd;
(4)①中为氨水和盐酸等体积等浓度混合,所得混合溶液中溶质为氯化铵,因为铵根发生水解,则溶液显酸性,pH<7,故答案为:<;
②中两溶液混合后pH=7,因为盐酸为强酸,氨水为弱碱,则需要氨水稍多一些,即氨水的浓度比盐酸的浓度大,c>0.2,因为溶液显中性,则所得混合溶液中各离子浓度大小关系为c(Cl-)=c(NH4+)>c(H+)=c(OH-),故答案为:>;c(Cl-)=c(NH4+)>c(H+)=c(OH-);
(5)若证明一水合氨是弱电解质,则可以从铵根能发生水解来说明,证明方案为:用玻璃棒蘸取0.1mol·L-1NH4Cl溶液滴在pH试纸上,显色后跟标准比色卡比较,测出pH,pH<7,故答案为:用玻璃棒蘸取0.1mol·L-1NH4Cl溶液滴在pH试纸上,显色后跟标准比色卡比较,测出pH,pH<7。


科目:高中化学 来源: 题型:
【题目】G是某抗炎症药物的中间体,其合成路线如下:
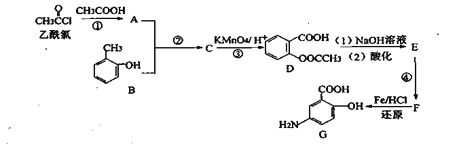
已知:①![]()
![]()
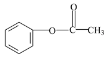
② ![]()
![]()
![]() (呈碱性,易氧化)
(呈碱性,易氧化)
(1)C的官能团名称是_______________;
(2)反应①的反应类型为___________;反应②的作用是___________________;
(3)下列对有机物G的性质推测不正确的是____________________ (填选项字母);
A.1molG与足量NaHCO3溶液反应放出2molCO2
B.能发生取代反应和氧化反应
C.能加聚合成高分子化合物
D.具有两性,既能与酸反应也能与碱反应
(4)写出E→F的化学反应方程式______________________________;
(5)同时符合下列条件的D的同分异构体有__________种:
①含有苯环且能发生水解反应:②能发生银镜反应;③能与NaHCO3溶液反应放出CO2。
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位:苯环上有发基时,新引入的取代基连在苯环的问位。根据题中的信息,写出以甲苯为原料合成有机物的流程图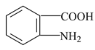 (无机试剂任选)_______________________________________________________________________________________。 合成路线流程图示例:X
(无机试剂任选)_______________________________________________________________________________________。 合成路线流程图示例:X![]() Y
Y![]() Z……目标产物
Z……目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________形象化描述。在基态原子中,核外存在______对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________。
(3)CS2分子中,共价键的类型有_____________,C原子的杂化轨道类型是_______,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____个六元环,每个六元环占有___个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________个六元环,六元环中最多有________个C原子在同一平面。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液浸润后,置于如图装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是( )
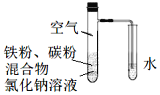
A.铁被氧化的电极反应式为Fe–3e=Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(1)用双线桥表示出电子转移的方向和数目__,题干中反应改写成离子方程式是___。
(2)电解食盐水的过程中,氧化产物是___。
(3)电解食盐水要求对粗食盐水进行精制,以除去租食盐水中含有的泥沙和SO42-、Ca2+,Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式:___,___。
(4)请配平以下化学方程式:__Al+__NaNO3+__NaOH=__NaAlO2+__N2↑+__H2O。若反应过程中转移5mol电子,则生成标准状况下N2的体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-苯基丙烯酸(俗名阿托酸)是一种重要的医药中间体、材料中间体,可用下列方法合成。首先,由A制得E,过程如下:
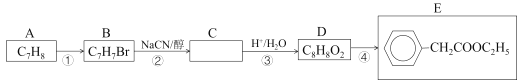
已知:i.CH3CH2Br+NaCN![]() CH3CH2CN+NaBr
CH3CH2CN+NaBr
ii.CH3CH2CN![]() CH3CH2COOH
CH3CH2COOH
(1)烃A的名称是___。D的同分异构体中,能发生银镜反应的芳香族化合物有多种,任写一种该类同分异构体的结构简式___。写出反应④的化学方程式___。
又已知,iii:R—CH2—COOCH2R’+HCOOCH2R”![]() +R”—CH2OH
+R”—CH2OH
然后,通过下列路线可得最终产品:
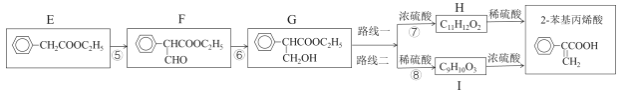
(2)检验F是否完全转化为G的试剂是___。反应⑤的化学方程式是___。
(3)路线二与路线一相比不太理想,理由是___。
(4)设计并完善以下合成流程图___。

(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三层(熔)液电解辉锑矿(Sb2S3,半导体)制取锑的装置如图所示。 下列说法错误的是( )
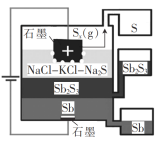
A.Sb在阴极生成
B.三层流体互不相溶,密度也不同
C.阳极的电极反应式为xS2- - 2xe- = Sx
D.该电解工艺可在室温下工作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,电子占据最高能层的符号为______,该能层上具有的原子轨道数为________,电子数为________。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?________(填“是”或“否”),原因是_____________________________________________ (如果前一问填“是”,此问可以不答)。
(3)镓与第ⅤA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子)。在GaAs晶体中,每个Ga原子与________个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为________。
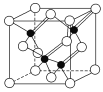
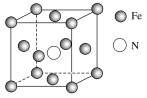
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为________;设晶胞边长为a cm,阿伏加德罗常数为NA,该晶体的密度为________ g·cm-3(用含a和NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com