
【题目】已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂,可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化.现有一课外活动兴趣小组利用上述设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率.若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL.试回答有关问题.
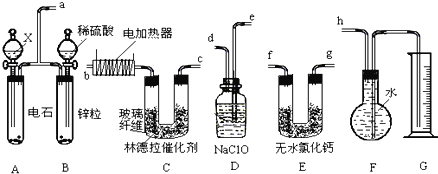
(1)所用装置的连接顺序是_______________(填各接口的字母).
(2)写出A、C中所发生的两个反应的化学方程式(有机物写结构简式):__________、_____________.
(3)为减慢A中的反应速率,X应选用_________.
(4)F中留下的气体除含少许空气外,还有________________.
(5)D的作用是_________________
(6)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_____________.
【答案】a、e、d、f、g、b、c、h(f、g可调换) CaC2+2H2O→HC≡CH↑+Ca(OH)2 HC≡CH+H2![]() CH2=CH2 饱和食盐水 H2、C2H4、C2H2 除去杂质气体 50%
CH2=CH2 饱和食盐水 H2、C2H4、C2H2 除去杂质气体 50%
【解析】
(1)根据实验的目的是用乙炔和氢气之间的反应来制取乙烯,根据装置的特点和应用来连接实验装置;
(2)碳化钙可以和水反应得到乙炔气体,乙炔气体和氢气在催化剂的作用下反应得到乙烯;
(3)为减慢反应速率,可以将水换成饱和食盐水;
(4)根据发生的反应结合实验实际情况来确定存在的杂质气体;
(5)乙炔在制取的过程中,还会含有杂质气体,要进行除杂;
(5)结合乙炔氢化的转化率等于反应的乙炔和全部的乙炔的量的比值来计算。
(1)实验装置显示制取乙炔和氢气,然后将二者混合,但是乙炔、氢气中含有杂质气体,应该先将杂质气体除去,再将之干燥,是纯净的气体在催化剂的作用下发生反应得到乙烯,乙烯是难溶于水的气体,可以采用排水法收集,所以装置的连接顺序是:a、e、d、f、g、b、c、h(f、g可调换),故答案为:a、e、d、f、g、b、c、h(f、g可调换);
(2)A中是碳化钙和水反应制取乙炔的过程,C中是乙炔和氢气之间的加成反应,方程式分别为:CaC2+2H2O→HC≡CH↑+Ca(OH)2、HC≡CH+H2![]() CH2=CH2,故答案为:CaC2+2H2O→HC≡CH↑+Ca(OH)2、HC≡CH+H2
CH2=CH2,故答案为:CaC2+2H2O→HC≡CH↑+Ca(OH)2、HC≡CH+H2![]() CH2=CH2;
CH2=CH2;
(3)碳化钙和水之间的反应十分剧烈,为减慢反应速率,可以将水换成饱和食盐水,故答案为:饱和食盐水;
(4)F中留下的气体除含少许空气外,还有没有完全消耗的乙炔,氢气以及生成的乙烯等气体,故答案为:H2、C2H4、C2H2;
(5)为了保证得到的气体纯净,应该将气体进行除杂,次氯酸钠具有碱性和氧化性,可以除去杂质,如果没有除去杂质,则剩余的气体增加,测得的结果比实际值偏高,故答案为:除去杂质气体;
(6)0.020molCaC2的电石,和水反应得到乙炔的物质的量是0.02mol,1.60g含杂质18.7%的锌粒(杂质不与酸反应)的物质的量是![]() mol=0.02mol,和硫酸反应,产生的氢气的物质的量是0.005mol,状况下测得G中收集到的水VmL,V=672mL,则得到的乙烯的物质的量是
mol=0.02mol,和硫酸反应,产生的氢气的物质的量是0.005mol,状况下测得G中收集到的水VmL,V=672mL,则得到的乙烯的物质的量是![]() =0.03mol,设乙炔的转化量是x,则有:
=0.03mol,设乙炔的转化量是x,则有:
HC≡CH+H2![]() CH2=CH2
CH2=CH2
1 1 1
x x x
则反应后得到气体的物质的量(0.02-x)+(0.02-x)+x=0.03,解得X=0.01mol,所以乙炔氢化的转化率为![]() ×100%=50%,故答案为:50%。
×100%=50%,故答案为:50%。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】一种铁-空气二次电池放电时氧原子的工作原理如图所示,电池反应为2Fe+O2+2H2O=2Fe(OH)2。下列有关该电池放电时的说法正确的是

A.能量由电能转变为化学能
B.电池工作时OH-由a极迁移向b极
C.b 极电极反应式为O2+4e-+4H+=2H2O
D.电子由a极经负载流向b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:
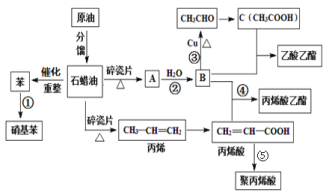
(1)A的结构简式为________________,丙烯酸中官能团的名称为___________________。
(2)写出下列反应的反应类型①___________________,②________________________。
(3)下列说法正确的是_____________。
A.硝基苯中混有浓HNO3和H2SO4,将其倒入到NaOH溶液中,震荡、静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.聚丙烯酸能够使酸性高锰酸钾溶液褪色
D.有机物C与丙烯酸属于同系物
(4)写出下列反应方程式:
③B→CH3CHO_________________________________________;
④丙烯酸 + B→丙烯酸乙酯_____________________;
⑤丙烯酸→聚丙烯酸_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈(Ce)是一种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、 Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:
(1)湿法空气氧化法回收铈的部分流程如下:(已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。)
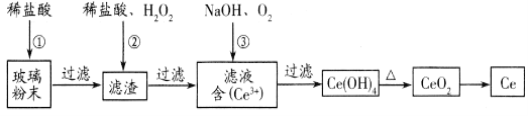
滤渣的成分是_____________________,反应②的离子方程式是_____________________________。
(2)干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为___________________________。
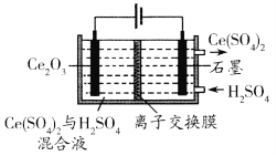
(3)利用电解方法也可以实现铈的回收。在酸性条件下电解Ce2O3(如图):阳极电极反应式为________________,离子交换膜为________ (填“阴”或“阳”)离子交换膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
(1)试推断写出它们的元素符号:A______,B______,C______,D______。
(2)画出D的离子结构示意图___________________。
(3)由这四种元素组成的三核10电子的分子式是_________ ,写出该分子的电子式 _________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列物质不能与二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤高氯酸 ⑥氢氧化钾 ⑦氧化钙⑧ 氮气
A.③⑤⑦⑧B.⑤⑦⑧C.⑤⑧D.⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含一定量Na2O杂质的Na2O2试样,用下图所示的实验装置通过与纯净、干燥的CO2反应来测定试样中Na2O2的纯度。
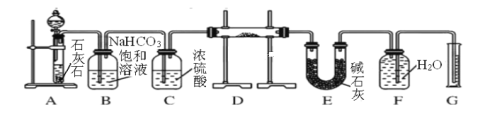
回答下列问题:
(1)按上图组装好实验装置后,首先应该进行的操作是______________。
(2)分液漏斗中所装试液是__________。
(3)装置D中发生反应的化学方程是:Na2O + CO2 = Na2CO3和____。
(4)E中碱石灰的作用是__________。
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则试样中Na2O2的含量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在好氧菌和厌氧菌作用下,废液中NH4+能转化为N2(g)和H2O(1),示意图如下:
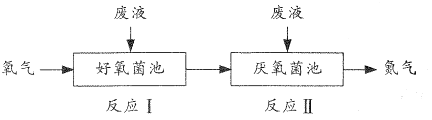
反应I:NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) △H1=akJ·mol-1
反应Ⅱ:5NH4+(aq)+3NO3-(aq)=4N2(g)+9H2O(l)+2H+(aq) △H2=bkJ·mol-1
下列说法正确的是
A.两池发生的反应中,氮元素只被氧化
B.两池中投放的废液体积相等时,NH4+能完全转化为N2
C.常温常压下,反应Ⅱ中生成22.4 L N2转移的电子数为3.75NA
D.4NH4+(aq)+3O2(g)=2N2(g)+6H2O(l)+4H+(aq) △H=![]() (3a+b) kJ·mol-1
(3a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.用石墨作电极电解MgCl2溶液:2H2O+2Cl-![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.过量的铁粉溶于稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O
C.用Na2S2O3溶液吸收水中的Cl2:4Cl2+S2O32-+5H2O=10H++2SO42-+8Cl-
D.SO2通入FeCl3溶液中:SO2+Fe3++2H2O=SO42-+Fe2++4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com