
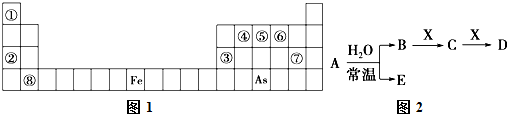
| A”¢“×Ėį |
| B”¢Ba£ØOH£©2 |
| CӢCO2 |
| DӢHF |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ĖłµĆČÜŅŗÖŠc£ØAg+£©”Įc£ØCl-£©£¾Ksp£ØAgCl£© |
| B”¢ĖłµĆČÜŅŗÖŠŠĪ³ÉĮĖøüÄѵēĄėµÄĪļÖŹ |
| C”¢ÉĻŹöŹµŃéĖµĆ÷Cl-ÓėNH4+¼äÓŠŗÜĒæµÄ½įŗĻĮ¦ |
| D”¢ÉĻŹö¹ż³ĢÖŠNH3?H2OµÄµēĄė³Ģ¶ČŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢25”ꏱ£¬0.1 mol?L-1 HFČÜŅŗÖŠpH=1 |
| B”¢Ksp£ØCaF2£©ĖęĪĀ¶ČŗĶ¹ĢĢåÖŹĮæµÄ±ä»Æ¶ų±ä»Æ |
| C”¢øĆĢåĻµÖŠĆ»ÓŠ³Įµķ²śÉś |
| D”¢ŌŚŌHFŗĶNaF»ģŗĻŅŗÖŠ£¬2c£ØNa+£©=c£ØF-£©+c£ØHF£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
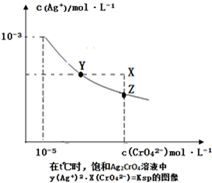 ŅŃÖŖt”ꏱAgClµÄKsp=4”Į10-l0£¬ŌŚt”ꏱ£¬Ag2CrO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ŅŃÖŖt”ꏱAgClµÄKsp=4”Į10-l0£¬ŌŚt”ꏱ£¬Ag2CrO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A”¢ŌŚt”ꏱ£¬Ag2CrO4µÄKspĪŖ1”Į10-11 |
| B”¢ŌŚ±„ŗĶČÜŅŗÖŠ¼ÓČėK2CrO4æÉŹ¹ČÜŅŗÓÉYµćµ½Zµć |
| C”¢ŌŚt”ꏱ£¬Ag2CrO4£Øs£©+2Cl-£Øaq£©?2AgCl£Øs£©+CrO42-£Øaq£©Ę½ŗā³£ŹżK=6.25”Į107 |
| D”¢ŌŚt”ꏱ£¬ŅŌ0.001mol/L AgNO3ČÜŅŗµĪ¶Ø20mL 0.001mol/L KClŗĶ0.001mol/LµÄK2CrO4µÄ»ģŗĶČÜŅŗ£¬CrO42-ĻČ³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢“óÓŚ10% | B”¢Š”ÓŚ10% |
| C”¢µČÓŚ10% | D”¢ĪŽ·Ø¼ĘĖć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
AӢ
| ||
BӢ
| ||
CӢ
| ||
DӢ
|
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com