
| A. | 只有① | B. | ①和③ | C. | ①②③ | D. | ①②③④ |
分析 ①1965年,中国科学家在世界上第一次用人工方法合成了结晶牛胰岛素;
②1897年,英国科学家汤姆生发现了电子;
③侯德榜发明了联合制碱法;
④首先制得氧气的是瑞典化学家舍勒;
⑤李比希最早提出元素的定量分析.
解答 解:①1965年,中国科学家在世界上第一次用人工方法合成了结晶牛胰岛素,故①正确;
②1897年,英国科学家汤姆生发现了电子,故②错误;
③侯德榜发明了联合制碱法,亦称侯氏制碱法,故③正确;
④首先制得氧气的是瑞典化学家舍勒,故④错误;
⑤最早提出有机物的元素的定量分析方法的是德国的化学家李比希,故⑤错误.
故选B.
点评 本题主要考查了化学史,难度不大,平时注意知识的积累.了解化学的发展史,有利于激发学生学习化学的兴趣,培养社会责任感.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
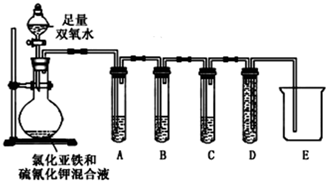
| 实验过程和象限 | 结论 |
| (2)试管A中盛有品红溶液;现象: 品红溶液褪色 | 证明气体中含有SO2 |
| (2)试管B中现象紫色酸性高锰酸钾溶液颜色不变或变浅 ;试管C中现象现象:澄清石灰水变浑浊 | 证明气体中含有CO2 |
| 实验过程 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
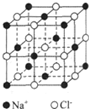 氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示;
氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④ | C. | ③④⑤ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W | Q |
| 原子半径/pm | 160 | 143 | 70 | 66 | 102 |
| 主要化合价 | +2 | +3 | +5、-3 | -2 | +6、-2 |
| A. | X、Y元素的金属性 X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 氢化物的沸点 H2W>H2Q |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com