
【题目】下列物质中,所含化学键种类最多的是
A.NaOHB.NH4ClC.CH3COONH4D.HC≡CH
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】下列各组溶液中的两个反应,可用同一离子方程式表示的是
A. BaCO3和HCl;BaCO3和H2SO4 B. BaCl2和H2SO4;Ba(OH)2和H2SO4
C. HNO3和K2CO3;HCl和NaHCO3 D. KOH和H2SO4;Ba(OH)2和HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、NO3-,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是

A. H+由右室进入左室
B. Ce4+从电解槽的c口流出,且可循环使用
C. 阴极的电极反应式:2HNO2+6H++6e-===N2↑+4H2O
D. 若用甲烷燃料电池作为电源,当消耗标准状况下33.6 L甲烷时,理论上可转化2mol HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁、高效新能源,也是重要的化工原料。
(1)工业上利用甲烷制备氢气的反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
已知:
①H2(g)+1/2O2(g)![]() H2O(g) △H1=-198kJ/mol
H2O(g) △H1=-198kJ/mol
②CO(g)+1/2O2(g)![]() CO2(g) △H2=-283kJ/mol
CO2(g) △H2=-283kJ/mol
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) △H3=-846.3kJ/mol
CO2(g)+2H2O(g) △H3=-846.3kJ/mol
则CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4=________。
CO(g)+3H2(g) △H4=________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g)![]() CH3OH(g) △H=-116kJ/mo1
CH3OH(g) △H=-116kJ/mo1
①如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是_______,理由_________;Y1_____Y2(填“<”“=”或“>”)。

②在2L恒容密闭容器中充入2 mol CO和4 mol H2,在一定条件下经过10 min达到平衡状态c点处。则在该条件下,从开始至达到平衡状态v(CH3OH)=_______________,平衡常数Ka、Kb、Kc 的大小关系:___________。
③下列措施既能增大反应速率又能提高反应物的转化率的是_______。
A.使用催化剂 B.及时分离CH3OH C.升高温度 D.增大压强
(3)已知燃料电池的比能量与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机物不论以何种比例混合,只要物质的量之和不变,那么完全燃烧时消耗的氧气的物质的量相等,且所生成的水的物质的量也相等的是( )
A. 甲烷和甲酸甲酯 B. 乙烷和乙酸
C. 乙炔和苯乙烯 D. 苯和苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一卤代烃RX与金属钠作用,可增加碳链制取高级烃,反应的化学方程式为:RX+2Na+![]() X→R—
X→R—![]() +2NaX。其中X代表卤原子,R和
+2NaX。其中X代表卤原子,R和![]() 为烃基,可以相同也可以不同。试以苯、乙炔、Br2、HBr、金属钠等为原料,通过三步反应制取
为烃基,可以相同也可以不同。试以苯、乙炔、Br2、HBr、金属钠等为原料,通过三步反应制取![]() ,写出制取过程的化学方程式。
,写出制取过程的化学方程式。
(1)______________________________________________________________;
(2)___________________________________________________________________;
(3)__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨对化学工业和国防工业具有重要意义。
(1)已知海水电解制得的氢气用于合成氨,某合成氨厂生产流程如下图:在第(3)个设备中用冷却的方法分离出液氨,其目的是:____________________________________________________________________。

(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为CH4(g)+H2O(g)CO(g)+3H2(g)(该反应为吸热反应),一定温度下,在体积为![]() 的恒容容器中发生上述反应,各物质的物质的量变化如表:
的恒容容器中发生上述反应,各物质的物质的量变化如表:
时间 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
①分析表中数据,判断![]() 时反应是否处于平衡状态?_______(填“是”或“否”,1分),前
时反应是否处于平衡状态?_______(填“是”或“否”,1分),前![]() 反应的平均反应速率
反应的平均反应速率![]() _______。
_______。
②在相同实验条件下,若改为加入![]() ,若要求平衡后
,若要求平衡后![]() 在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为__________________________
在反应混合气中质量分数不变,则还需加入CO、H2、H2O这三种物质对应的物质的量分别为__________________________
③反应在![]() 内,
内,![]() 的物质的量减少的原因可能是_______(填字母)。
的物质的量减少的原因可能是_______(填字母)。
![]() .减少
.减少![]() 的物质的量
的物质的量 ![]() .降低温度
.降低温度 ![]() .升高温度
.升高温度 ![]() .充入
.充入![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等明显药效的健康食品。苹果酸(2羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为
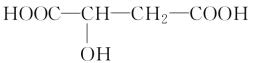
下列相关说法不正确的是( )。
A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.1 mol苹果酸与足量Na反应生成33.6 L H2(标准状况下)
D.1 mol苹果酸与Na2CO3溶液反应一定消耗2 mol Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com