
分析 (1)氧气浓度变化量为$\frac{0.4mol}{2L}$=0.2mol/L,根据υ=$\frac{△c}{△t}$计算υ(O2),再根据速率之比等于化学计量数之比计算υ(NO2);
(2)由方程式可知△n(N2O5)=2△n(O2),进而计算N2O5转化率.
解答 解:(1)氧气浓度变化量为$\frac{0.4mol}{2L}$=0.2mol/L,则υ(O2)=$\frac{0.2mol/L}{5min}$=0.04 mol/(L•min),速率之比等于化学计量数之比,则υ(NO2)=4υ(O2)=0.16 mol/(L•min),
答:υ(NO2)=0.16 mol/(L•min),υ(O2)=0.04 mol/(L•min);
(2)由方程式可知△n(N2O5)=2△n(O2)=0.4mol×2=0.8mol,则N2O5转化率=$\frac{0.8mol}{4mol}$×100%=20%,
答:5min时,N2O5的转化率为20%.
点评 本题考查化学平衡计算,比较基础,旨在考查学生对基础知识的巩固.


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:解答题
 碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.| 时间/min 浓度/mol/L | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图②中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| B. | 图①表示25℃时,用0.1mol•L-1盐酸滴定20mL 0.1mol•L-1NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 图③表示10mL 0.01mol•L-1 KMnO4 酸性溶液与过量的0.1mol•L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
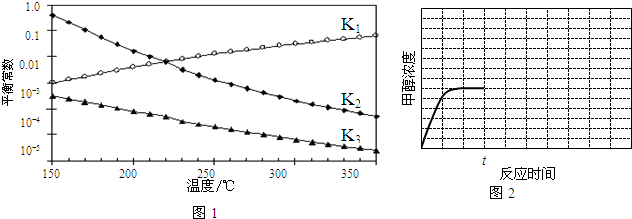
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
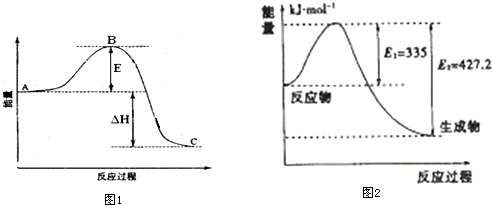
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| IE1 | IE2 | IE3 | IE4 | IE5 | IE6 |
| 11 | 24 | 48 | 64 | 392 | 490 |
| A. | B | B. | C | C. | N | D. | O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L煤油(假定化学式为C8H18)中含有0.8NA个碳原子 | |
| B. | 常温常压下,O2和O3的混合物16g中含有NA个氧原子 | |
| C. | 25℃时,1L 0.1mol•L-1的氢氧化钠溶液中含有NA个OH- | |
| D. | 0.5mol CH4中含有0.5NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com