
乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品。已知乙烯能发生以下转化:

(1)乙烯的结构简式为 。
(2)反应①的反应类型是 ,D中含官能团名称为 。
(3)写出以下反应的化学方程式:
① ;
② ;
③ 。
(4)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:
工艺二:
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,在实际生产中,应采用
(填“工艺一”或“工艺二”)更环保、更经济。
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式: 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | ; |
| 步骤2:____________________________________ ____________________________________。 |
|
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:
取少量样品溶于水, 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律表述正确的是
A.原子序数为15的元素的最高化合价为+3
B.第ⅦA族元素是同周期中非金属性最强的元素
C.Li、Na、K、Rb、Cs的得电子能力逐渐增强
D.原子序数为12的元素位于元素周期表的第三周期的ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下列述叙正确的是
A.取一小块铝箔用砂纸打磨除去表面的氧化膜后,在酒精灯上加热灼烧,可看到铝箔燃烧起来火星四溅
B.Mg(OH)2的悬浊液中加入NH4Cl溶液后变澄清,是因为Mg(OH)2的Ksp在NH4Cl溶液中变大
C.将0.01mol/LKMnO4的酸性溶液滴入0.1mol/LH2C2O4溶液中,紫红色褪去的速率会逐渐加快
D.将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
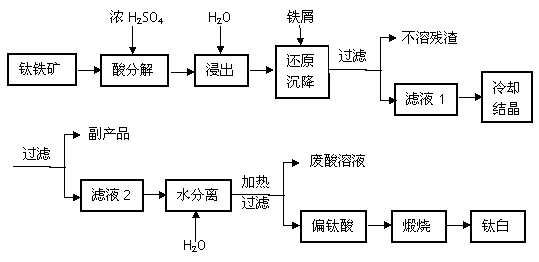
工业常用浓硫酸分解钛铁矿FeTiO3(含有FeO、Fe2O3杂质)方法来制备钛白(TiO2)工艺流程如下图所示。
 金属钛具有密度小、比强度高、耐腐蚀(如酸或碱)、无毒等优点,已广泛应用于航天工业,并逐步进入了化工、船舶、汽车等领域,并显示了巨大的发展潜力。工业上冶炼常用还原法由钛白得到金属钛。主要的工艺流程如下图所示。
金属钛具有密度小、比强度高、耐腐蚀(如酸或碱)、无毒等优点,已广泛应用于航天工业,并逐步进入了化工、船舶、汽车等领域,并显示了巨大的发展潜力。工业上冶炼常用还原法由钛白得到金属钛。主要的工艺流程如下图所示。


回答下列问题:
(1)浓硫酸处理钛铁矿时生成两种硫酸盐且无气体放出,写出FeTiO3(Fe+2价)在浓硫酸中分解的反应方程式_____________________________________________________;
(2)加铁屑的目的是___________________________________(用离子方程式表示),滤液1冷却结晶得到副产品的俗称是______________________(写名称);
(3)滤液2稀释加热水解得到偏钛酸(H2TiO3)的方程式______________________________;
(4)冶炼金属钛时反应①通常在800~900℃的条件下进行,产物中还有一种可燃性无色气体,该反应的方程式为______________________________________________________。
(5) 冶炼金属钛时反应②也在800~900℃的条件下进行,反应中需要加入氩气的理由是___________________;反应后的产物中需要加入_____________才能达到分离的目的。
(6)已知25℃、100kPa时TiCl4为液态,实验测得该条件下12g镁反应能释放出266.1kJ 热量,反应②的热化学方程式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的叙述正确的是
A.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别
B. 除去乙烷中少量的乙烯,可在光照条件下通入Cl2,再气液分离
C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
D.蛋白质、葡萄糖、油脂均能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅴ是具有抗氧化和抗肿瘤作用成分.化合物Ⅴ也可通过图所示方法合成:


已知 、
、
(1)反应①的类型________
(2)化合物Ι的分子式________
(3) ①A的结构简式_______。
② 1molV最多消耗NaOH ____。1mol肉桂酸最多消耗H2 _______mol
(4)化合物I和Ⅱ反应还可以得到一种酯,该反应的化学方程式是
(5)关于Ⅴ的说法正确的是( )
A.分子中有三个苯环 B.能发生水解反应
C.使酸性KMnO4溶液褪色 D.与FeCl3发生显色反应
(6)写出肉桂酸的一种同分异构体的结构简式 ,满足一下两个条件:
①分子中含有苯环 ②羧基与苯环直接相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com