
【题目】观察下列几个装置示意图,有关叙述不正确的是( )
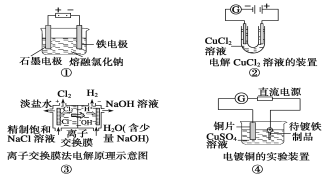
A.装置①工业上可用于生产金属钠,电解过程中石墨电极产生氯气,此法也可用于生产活泼金属镁、铝等
B.装置②中随着电解的进行右边电极会产生红色的铜,并且电流计示数不断变小
C.装置③中的离子交换膜具有很强的选择性,只允许某类离子(如Na+)通过
D.装置④的待镀铁制品应与电源负极相连
科目:高中化学 来源: 题型:
【题目】“题18图”为两物质的溶解度曲线。请回答:
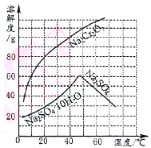
(1)50℃时,Na2Cr2O7的溶解度为________g;60℃时溶解度:Na2Cr2O7__________Na2SO4(填“<”、“=”、“>”)。
(2)在50℃时,把210gNa2Cr2O7饱和溶液降温到10℃时,析出Na2Cr2O7______________g (假设不含结晶水)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜在自然界中常以多种形态存在,现以孔雀石矿石[成分为Cu2(OH)2CO3、CuFeS2、SiO2、Fe2O3等]为原料生产主产品胆矾和副产品铁红的工艺流程如图:
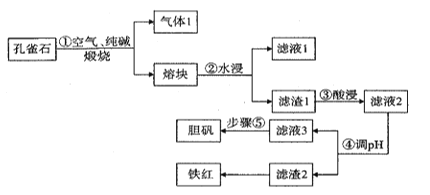
(1)气体1的成分除H2O(g)外,还有_______________,步骤①中发生氧化还原反应的化学方程式为 ___________________________________________________,滤液1的主要成分的用途之一为________________________________________。
(2)目前工业生产中步骤③酸浸的百分率为70%,为进一步提高酸浸的百分率可采取的措施有__________(答出两点)。
(3)步骤④调pH所用试剂为_____________ 。
(4)室温下滤液3的pH=4,Ksp[Fe(OH) 3]=4×10-38,则滤液3中c(Fe3+)=____________。
(5)步骤⑤操作为___________________________________________________________.。
(6)假设使用孔雀石质量为m kg,步骤③酸浸的百分率为70%,经滤渣2所得铁红的质量为n kg,则孔雀石矿石中铁元素的含量为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中的能量转化不正确的是( )
选项 | 化学反应 | 能量转化形式 |
A | CH4+2O2 | 化学能转化成热能 |
B | Pb+PbO2+2H2SO4 | 使用时放电,电能转化成化学能 |
C | mH2O+nCO2 | 光能转化成化学能 |
D | CaCO3 | 热能转化成化学能 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写下列反应的方程式:
(1)NO2溶于水的化学反应方程式:__。
(2)实验室制取氨气的化学反应:__。
(3)乙醇与乙酸的酯化反应方程式:__。
(4)红热的碳和浓硝酸的化学反应方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是来自石油的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。根据如图转化关系完成下列各题:
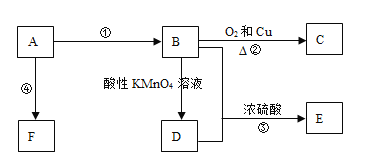
(1)A的分子式是__,C的名称是__,F的结构简式是__。
(2)D分子中的官能团名称是__,请设计一个简单实验来验证D物质存在该官能团,其方法是__。
(3)写出反应②的化学方程式并指出③的反应类型:
反应②:__;反应③类型是__反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
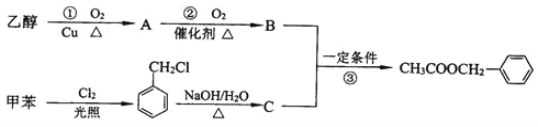
(1)A的名称为___;C的结构简式为___;
(2)写出反应①的化学方程式___;
(3)反应③的反应类型为___;
(4)C通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的同分异构体的结构简式(各写一种)___;___。
(5)反应__(填序号)原子的理论利用率为100%,符合绿色化学的。
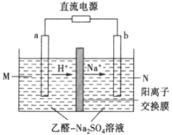
(6)一种处理高浓度乙醛废水的方法——隔膜电解法,其原理如图所示,电解质溶液为一定浓度含乙醛的Na2SO4溶液,电解后乙醛在两个电极分別转化为乙醇和乙酸。写出阳极电极式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
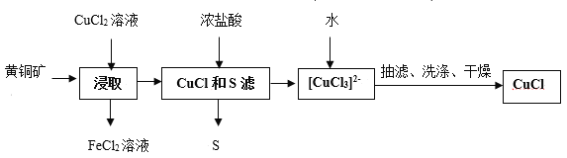
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)(无色溶液)
[CuCl3]2-(aq)(无色溶液)
下列叙述错误的是( )
A.浸取中的主要反应为CuFeS2+3CuCl2=4CuCl+FeCl2+2S
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s)+2Cl(aq)-![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl
[CuCl3]2-(aq)平衡逆向移动,析出CuCl
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com