
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 残留固体成分 | Fe、Cu | Cu | Cu | - | - | - |
| 溶液中的金属离子 |
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 溶液中的金属离子 | Fe2+ | Fe2+ | Fe2+、Cu2+ | Fe2+、Cu2+ | Fe2+、Fe3+、Cu2+ | Cu2+、Fe3+ |


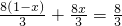 mol;
mol;
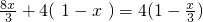 mol
mol


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 残留固体成分 | Fe、Cu | Cu | Cu | - | - | - |
| 溶液中的金属离子 |
| 8 |
| 3 |
| x |
| 3 |
| 8 |
| 3 |
| x |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用粒子符号填写下列空白(列举出全部可能的情况)
| ① | ② | ③ | ④ | … |
残留固体成分 |
|
|
|
|
|
溶液中的金属离子 |
|
|
|
|
|
(2)当溶液中金属离子只有Fe2+和Cu2+时,则b的取值范围是__________________(用a、x表示)。
(3)当x=0.5,溶液中Fe3+与Fe2+的物质的量相等时,在标准状况下共产生672 mL气体。求a、b的值。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有六种情况,请用粒子符号填写下列空白:
| ① | ② | ③ | ④ | ⑤ | ⑥ |
溶液中的金属离子 |
| Fe2+ |
| Fe2+ Cu2+ |
| Cu2+ Fe3+ |
残留固体成分 | Fe Cu |
| Cu | — | — | — |
(2)当溶液中金属离子只有Fe2+、Cu2+时,求b的取值范围。?
查看答案和解析>>
科目:高中化学 来源:2015届上海市浦东新区高二上学期期末考试化学试卷(解析版) 题型:填空题
现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的量分数为x;研成粉末后,全部投入含b mol HNO 的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为__________。(写出所有可能情况)
(2)当溶液中金属离子只有Fe 、Cu
、Cu 时,则b的取值范围是(用a、x表示)___________。
时,则b的取值范围是(用a、x表示)___________。
(3)当x=0.5,溶液中Fe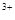 与Fe
与Fe 的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为amol,Cu的物质的量分数为x;研成粉末后,全部投入含bmol HNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:(已知:Cu+2Fe3+=2Fe2++Cu2+)
(1)随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有六种情况,请用粒子符号填写下列空白:
| ① | ② | ③ | ④ | ⑤ | ⑥ |
溶液中的金属离子 |
| Fe2+ |
| Fe2+、Cu2+ |
| Cu2+、Fe3+ |
残留固体成分 | Fe、Cu |
| Cu | ―― | ―― | ―― |
(2)当溶液中金属离子只有Fe2+、Cu2+时,求b的取值范围。
(3)当x=0.5时,溶液中Fe3+与Fe2+的物质的量相等时,在标准状况共产生672mL气体。求a、b的值。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com