解答:解:A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素.A是形成化合物种类最多的元素,则A为碳元素;B原子基态电子排布中只有一个未成对电子,外围电子排布为ns
2np
1或ns
2np
5,结合原子序数且B为非金属性元素,可推知外围电子排布为ns
2np
5,C是同周期元素中原子半径最小的元素,处于ⅦA族,可推知B为F元素、C为Cl元素;D的基态原子在前四周期元素的基态原子中单电子数最多,其原子外围电子排布式为1s
22s
22p
63s
23p
63d
54s
1,则D为Cr;E与D相邻,E的某种氧化物X与HCl的浓溶液加热时反应常用于实验室制取气态单质Cl
2,则E为Mn、X为MnO
2;F与D的最外层电子数相等,最外层电子排布为ns
1,原子序数大于Cr,则F为Cu,
(1)D的基态原子在前四周期元素的基态原子中单电子数最多,其核外电子排布式:1s
22s
22p
63s
23p
63d
54s
1,故答案为:1s
22s
22p
63s
23p
63d
54s
1;
(2)HF分子间能形成氢键,故其沸点比较HCl高,故答案为:高;HF分子间能形成氢键;
(3)同周期自左而右电负性增大,故电负性C<F,C
2H
4中C原子成2个C-H、1个C=C双键,不含孤对电子,C原子采取sp
2杂化,故答案为:小于;sp
2;
(4)MnO
2在制取Cl
2单质中的作用是氧化剂,C的某种含氧酸盐常用于实验室中制取氧气,此酸根离子为ClO
3-,Cl原子价层电子对数=3+
=4,含有1对孤对电子,为三角锥形,故化学键的键角<109°28′,
故答案为:氧化剂;<;
(5)由晶胞结构可知,晶胞中黑色球数目=4、白色球数目=8×
+6×
=4,故该化合物的化学式是CuCl,晶胞的质量=4×
g,晶胞中黑色球与周围的4个白色球形成正四面体结构,若Cu与Cl原子最近的距离为a cm,如图正四面体:
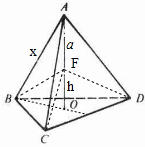
,连接F与A、B、C、D,则三棱锥A-BCD均分为等4个等体积的三棱椎,则V
三棱锥A-BCD=4V
三棱锥F-BCD=,故
S
△BCD?(a+h)=4×
S
△BCD?h,故h=
a,令正四面体的棱长为x cm,连接AF并延长交三角形BCD与O,O为正三角形BCD的中心,BO垂直平分CD,则BO的长度=x cm×
×
=
cm,在直角三角形BOF中,(
)
2+(
a)
2=a
2,解得x=
,故晶胞的棱长=
×2x cm=
×2×
cm=
cm,故晶胞的体积=(
cm)
3=
a
3 cm
3,则晶胞密度=
=
g?cm
-3,
故答案为:
.


 ,连接F与A、B、C、D,则三棱锥A-BCD均分为等4个等体积的三棱椎,则V三棱锥A-BCD=4V三棱锥F-BCD=,故
,连接F与A、B、C、D,则三棱锥A-BCD均分为等4个等体积的三棱椎,则V三棱锥A-BCD=4V三棱锥F-BCD=,故

 阅读快车系列答案
阅读快车系列答案 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.