
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 先根据题干信息“烷烃主链上有4个碳原子的同分异构体有2种”确定烷烃的分子式,然后再根据官能团位置异构确定烯烃的同分异构体,据此进行解答.
解答 解:先确定该烷烃碳原子个数:
①主链为4个碳原子的烷烃,其支链只能是甲基(不可能是乙基,否则主链超过4个碳原子);
②主链为4个碳原子的烷烃,支链数最多4个(下面的0,是指该物质只有一种,没有同分异构体)
甲基的个数 同分异构体
1个 0
2个 2
3个 0
4个 0
根据分析可知,该烷烃总共有6个碳原子,则满足条件的烯烃的同分异构体数目为:
①双键在1号位,有以下3种
C=C-C-C
1 2 3 4
2-乙基丁烯、2,3-二甲基丁烯、3,3-二甲基丁烯,总共有3种;
②双键在2号位,有1种:
C-C=C-C
1 2 3 4
2,3-二甲基-2-丁烯
根据以上分析可知,满足条件的烯烃总共有4种,
故选A.
点评 本题考查了同分异构体的书写方法,题目难度不大,根据信息确定烷烃分子中含有C原子数为解答关键,注意掌握同分异构体的书写原则,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 用CH3COOH溶解CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 氯化铝溶液中滴加过量氨水Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- | |
| D. | 过量二氧化碳通入偏铝酸钠溶液中CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
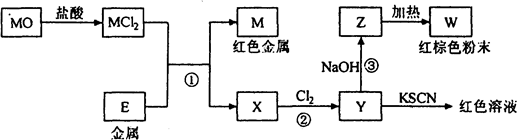
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融电解质中,O2-由正极移向负极 | |
| B. | 当负极消耗4.48L气体时,转移电子5.2mole- | |
| C. | 电子的流动方向:负极经外电路流向正极,再通过内电路流回负极 | |
| D. | 通入丁烷的一极是负极,电极反应为:C4H10-26e-+13O2-═4CO2+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ④
④ 等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.
等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
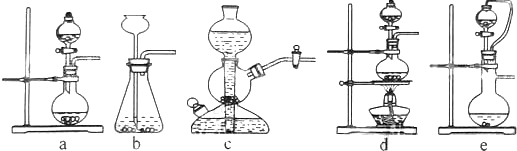
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com