
| A. | 氯化氢的电子式为 H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| B. | 乙炔的结构简式(删:可以)写成 CHCH | |
| C. | 镁的原子结构示意图 | |
| D. | 碳酸氢钠溶于水电离方程式:NaHCO3═Na++H++CO32- |
分析 A.氯化氢属于共价化合物,分子中不存在阴阳离子;
B.结构简式碳碳三键不能省略;
C.在原子结构示意图中,圆圈表示原子核,圆圈内的数值为质子数,核外电子层用弧线表示,弧线上的数据表示每层的电子数;
D.碳酸氢钠为强电解质,完全电离生成钠离子和碳酸氢根离子,碳酸氢根离子不能完全电离.
解答 解:A.HCl为共价化合物,是由H和Cl通过共用电子对结合在一起的,其正确的电子式为: ,故A错误;
,故A错误;
B.乙炔的结构简式CH≡CH,故B错误;
C.镁元素含有12个质子,原子核外有12个电子,分三层排布,原子结构示意图为 ,故C正确;
,故C正确;
D.碳酸氢钠为多元弱酸的酸式盐,碳酸氢根离子不能完全电离,所以碳酸氢钠溶于水的电离方程式为NaHCO3═Na++HCO3-,故D错误;
故选C.
点评 本题考查了常见化学用语的书写判断,题目难度不大,注意掌握电子式、结构简式、原子结构示意图、电离方程式等化学用语的书写原则,明确离子化合物与共价化合物的电子式的区别,试题培养了学生规范答题的能力.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
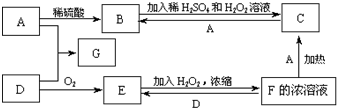 中学化学中几种常见物质的转化关系如图(有部分产物未画出).A是一种金属单质,D是一种非金属固体单质.
中学化学中几种常见物质的转化关系如图(有部分产物未画出).A是一种金属单质,D是一种非金属固体单质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作水果的催熟剂 | |
| B. | 甘油可用于护肤用品 | |
| C. | 料酒可以除去食物中的腥味 | |
| D. | 裂化汽油可用作提取碘水中碘的萃取剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LHF分子中所含的原子数约为2NA | |
| B. | 1mol冰中,平均所含氢键的数目为NA | |
| C. | 在氧化还原反应中,1molH2O2转移的电子数为2NA | |
| D. | 13gCnHn分子中最多含C-C数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解,则溶液中一定有Cl- | |
| D. | 加入KSCN,溶液变血红色,则溶液中一定有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com