
下列叙述错误的是()
A. 10ml质量分数为98%的H2SO4,用10ml水稀释后,H2SO4的质量分数大于49%
B. 配制0.1mol/L的Na2CO3溶液480ml,需用500ml容量瓶
C. 在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水
D. 向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变)
考点: 溶液中溶质的质量分数及相关计算;溶液的配制.
专题: 物质的量浓度和溶解度专题.
分析: A.浓硫酸的密度ρ1大于水的密度ρ2,浓度越大密度越大;
B.实验室没有480mL的容量瓶,应用500mL的容量瓶进行配制;
C.根据c=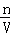 ,体积V指的是溶液的体积,而不是溶剂水的体积;
,体积V指的是溶液的体积,而不是溶剂水的体积;
D.发生反应:2Na2O2+2H2O═4NaOH+O2↑,Na2O+H2O═2NaOH,由方程式可知,相同物质的量的Na2O2和Na2O的消耗相同物质的量的水,生成相同物质的量的NaOH,保持温度不变,使溶液恰好饱和,故加入的Na2O2、Na2O的物质的量相等.
解答: 解:A.浓硫酸的密度ρ1大于水的密度ρ2,加水后浓硫酸质量分数= ×100%=
×100%=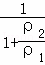 >49%,故A正确;
>49%,故A正确;
B.实验室没有480mL的容量瓶,应用500mL的容量瓶进行配制,根据n=cV、m=nM进行计算,故B正确;
C.在标准状况下,22.4L氨气的物质的量为1mol,配成1L溶液而不是溶于1L水中,得到1mol/L的氨水,故C错误;
D.若要生成80份质量的氢氧化钠,需要78份质量的过氧化钠,同时消耗18份质量的水,需要62份质量的氧化钠,同时消耗18份质量的水,则加入的Na2O2与Na2O的物质的量之比等于1:1,故D正确;
故选C.
点评: 本题考查溶液浓度计算、基本操作,注意理解掌握物质的量浓度与质量分数之间的关系.注意实验室常用容量瓶的规格,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: .
(2)以甲烷为原料制取氢气是工业上常用的制氢方法.
已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学科学的叙述中,正确的是()
A. 化学学科与其他学科分支的联系不紧密
B. 化学知识只是在工业生产中起到重要作用
C. 化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中
D. 化学科学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的重要自然科学
查看答案和解析>>
科目:高中化学 来源: 题型:
将钠、镁、铝各0.3mol分别加入100mL 1mol/L 的盐酸中,在同温同压下产生的气体体积比是()
A. 1:2:3 B. 6:3:2 C. 3:1:1 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
日常生活中很多问题涉及到化学知识.下列叙述正确的是()
A. 用食醋清洗热水瓶中的水垢;用米汤检验碘盐中含有碘酸钾
B. 用小苏打可中和胃酸,热纯碱溶液可除油污.小苏打和纯碱可以用石灰水鉴别
C. “84消毒液”和洁厕剂能同时使用,除污垢效果好
D. 用丁达尔效应区别鸡蛋白溶液和食盐水;用明矾可以净水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的制备合理的是()
①将氯化铝与硫化钾溶液混合后过滤来制备硫化铝
②将过量的铁与氯气加热反应制备氯化亚铁
③在配制的硫酸亚铁溶液常加入一定量的铁粉和硫酸
④铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
⑤将45mL水加入到盛有5g氯化钠的烧杯中,溶解配制50g质量分数为5%的氯化钠溶液.
A. 只有④ B. 只有②③ C. 只有③④ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
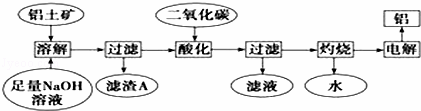
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的Na2SiO3与Na2与 反应,能生成硅铝酸盐沉淀,化学反应方程式为:
反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2Na2═2Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中主要发生反应的离子方程式: ; .
(2)滤渣A的主要成分为 ;滤渣A的用途是(只写一种) .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氧化物的叙述不正确的是()
①非金属氧化物不一定属于酸性氧化物
②酸性氧化物都属于非金属氧化物
③金属氧化物都属于碱性氧化物
④碱性氧化物都属于金属氧化物
⑤酸性氧化物都能与水反应生成相应的含氧酸
⑥两性氧化物既能与酸也能与碱反应生成盐和水
⑦不能与酸反应的氧化物一定能与碱反应
⑧与水反应生成含氧酸的氧化物一定是酸性氧化物.
A. ①②③⑥⑧ B. ②③⑤⑦⑧ C. ②③⑤⑥⑦ D. ②③④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象说法正确的是()
A. 红热的铁丝在氯气中燃烧产生棕色的烟雾
B. 含有氯元素的物质都呈黄绿色
C. 氢气在氯气中燃烧时火焰呈淡蓝色,在瓶口有白雾产生
D. 钠在空气里加热,先熔成小球,剧烈燃烧,产生黄色火焰,生成淡黄色固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com