
A.CH2═CH2![]() CH3CH2Cl B.CH3CH3
CH3CH2Cl B.CH3CH3![]() CH3CH2Cl
CH3CH2Cl
C.CH3CH2OH![]() CH3CH2Cl D.CH2ClCH2Cl
CH3CH2Cl D.CH2ClCH2Cl![]() CH3CH2Cl
CH3CH2Cl
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

![]()


上述反应中,关于(Ⅰ)、(Ⅱ)两步的反应类型,正确的是( )
A.化合反应,分解反应 B.加成反应,水解反应
C.还原反应,分解反应 D.氧化反应,水解反应
(2)在上述化合物中,左旋多巴(C)属于氨基酸,它具有两性,即:既有酸性,又在
碱性。因此,它们只是与下列物质中的( )不进行反应。
A.金属钠 B.氢氧化钠 C.氯化钠 D.盐酸
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省襄阳市高三元月第一次调研考试理综化学试卷(解析版) 题型:填空题
近年来,为提高能源利用率,西方提出共生理念——为提高经济效益,人类生产活动尽可能多功能化.共生工程将会大大促进化学工业的发展.
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V.实际过程中,将SO2通入电池的 极(填“正”或“负”),负极反应式为 .用这种方法处理SO2废气的优点是 .
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如下:
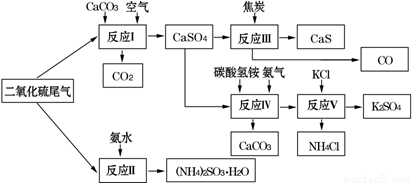
①生产中,向反应Ⅱ中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 .
②下列有关说法正确的是 .
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为CaSO4+4C  CaS+4CO↑
CaS+4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
③反应Ⅴ中选用了40%的乙二醇溶液做溶剂,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液做溶剂的原因是 .
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
A.CH2=CH2![]() CH3CH2Cl B.CH3CH3
CH3CH2Cl B.CH3CH3![]() CH3CH2Cl
CH3CH2Cl
C.CH3CH2OH![]() CH3CH2Cl D.CH2ClCH2Cl
CH3CH2Cl D.CH2ClCH2Cl![]() CH3CH2Cl
CH3CH2Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com