
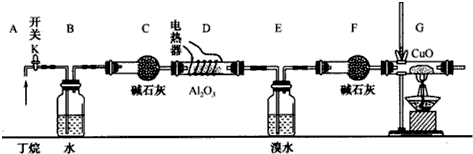

分析 (1)应先检验气密性,赶出内部气体,再加热;
(2)在装置G的末端收集一小试管气体堵住管口,靠近火焰,松开手指,若没有爆鸣声,则空气排尽;
(3)通过观察气泡,控制气体流速;
(4)根据裂解方程式可知,CH4的物质的量等于C3H6的物质的量,C2H6的物质的量等于C2H4的物质的量,E、F吸收的是烯烃,G减少的质量是氧化铜中的氧元素质量,丁烷的裂解中,生成乙烯的物质的量和乙烷的物质的量相等,甲烷和丙烯的物质的量相等,再结合原子守恒计算甲烷和乙烷的物质的量之比;
(5)分离不互溶的液体用分夜,分离互溶的液体用蒸馏.Na2SO3溶液可吸收溴单质.
解答 解:(1)应先检验气密性,赶出内部气体,再给D、G装置加热;
故答案为:②③①;
(2)在装置G的末端收集一小试管气体堵住管口,靠近火焰,松开手指,若没有爆鸣声,则空气排尽;
故答案为:打开K,使丁烷气依次流经各装置,在装置G的末端收集一小试管气体堵住管口,靠近火焰,松开手指,若没有爆鸣声,则空气排尽;
(3)B装置所起的作用是通过观察气泡,控制气体流速;
故答案为:通过观察气泡,调节K,控制气体流速;
(4)E、F吸收的是烯烃,G减少的质量是氧化铜中的氧元素质量,丁烷的裂解中,生成乙烯的物质的量和乙烷的物质的量相等,甲烷和丙烯的物质的量相等,再结合原子守恒计算甲烷和乙烷的物质的量之比,所以要测定E、F在反应前后的质量差及G在反应前后的质量差,
故答案为:E、F,G;
(5)亚硫酸钠与有机物不互溶,分离不互溶的液体用分夜;分离互溶的液体用蒸馏,Na2SO3溶液可吸收溴单质,反应的离子方程式为SO32-+Br2+H2O═SO42-+2H++2Br-,
故答案为:分液; 蒸馏;SO32-+Br2+H2O═SO42-+2H++2Br-.
点评 本题以丁烷裂解为载体考查实验基本操作、计算、物质的分离和提纯,明确流程图中各个装置的作用、物质分离和提纯方法的选取等知识点即可解答,题目难度中等.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
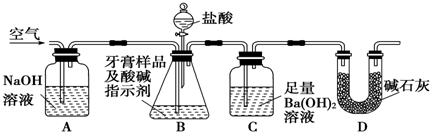
| 实验步骤 | 预期现象与结论 |
| 取适量牙膏样品于试管中,加入足量的NaOH溶液,过滤, 向滤液中滴加盐酸. | 滤液中先出现白色沉淀, 随后沉淀溶解,说明该牙膏摩擦剂中含氢氧化铝. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | 电离常数 |
| H2SO3 | K1=1.3×10-2,K2=6.2×10-8 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量、不同密度的N2和CO | B. | 同温度、同体积的H2和N2 | ||
| C. | 同体积、同密度的C2H6和NO | D. | 同压强、同体积的N2O和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
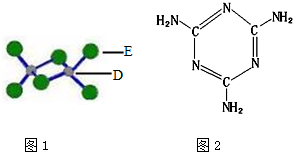 A、B、C、D、E为原子序数依次增大的短周期元素,B、C相邻且同周期,C原子中含有8种运动状态不同的电子.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.D是地壳中含量最多的金属元素.E元素为同周期电负性最大的元素.E和D可形成化合物丙.F为第四周期未成对电子数最多的元素
A、B、C、D、E为原子序数依次增大的短周期元素,B、C相邻且同周期,C原子中含有8种运动状态不同的电子.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.D是地壳中含量最多的金属元素.E元素为同周期电负性最大的元素.E和D可形成化合物丙.F为第四周期未成对电子数最多的元素查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天津港爆炸案中对剧毒的氰化钠(NaCN) 喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| B. | 碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应 | |
| C. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 | |
| D. | 石油原油的脱水,有色玻璃、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用磁铁分离出混合物中的铁粉 | B. | 将混合物溶于二硫化碳后过滤 | ||
| C. | 将混合物溶解于稀盐酸后过滤 | D. | 将混合物加热升华 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com