
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,设计 如右图所示的电池装置:

①该电池的能量转化形式为 。
②该电池正极的电极反应为 。
③工作一段时间后,测得溶液的pH减小,则该电池总反应的化学方程式为 。
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
常温下,pH=12的氨水中存在以下电离平衡:NH3·H2O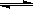 NH4++OH—。往其中加入少量 0.01mol·L-1NaOH溶液,保持不变的是
NH4++OH—。往其中加入少量 0.01mol·L-1NaOH溶液,保持不变的是
A.c(OH—) B.c(NH4+) C.c(NH3·H2O) D.c(NH4+)·c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.合金的熔点一般比组成合金的各成分金属高
B.我国规定商家不得无偿提供塑料袋,目的是降低成本
C.红宝石、蓝宝石和金刚石都是由碳元素组成的宝石
D.氮化硅、光导纤维、氧化铝陶瓷等属于新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
根据化学学科中的基本理论,请回答下列问题:
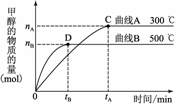 I、常温下,取pH=2的盐酸和醋酸溶液各100 ml, 向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是_____ (填“A”或“B”)。
I、常温下,取pH=2的盐酸和醋酸溶液各100 ml, 向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是_____ (填“A”或“B”)。
II、丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
 已知:
已知:
(1)写出丙烷的燃烧热的热化学方程式:
(2)现有1mol C3H8在不足量的氧气里燃烧,生成1mol CO和2mol CO2以及气态水,将所有的产物通入一个固定体积为1L的密闭容器中,在一定条件下发生如下可逆反应:
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化 b.v正(H2) = v逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再反生变化
②5min后体系达到平衡,经测定,H2为0.8mol,则v(H2)= 。
③向平衡体系中充入少量CO,则平衡常数 (填“增大”、“减小”或“不变”)。
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-。在电池内部O2-移
向 极(填“正”或“负”);电池的正极电极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铜锌原电池(右图)的叙述正确的是
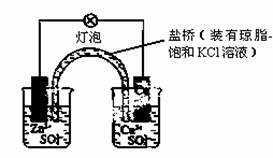
A.正极反应为Zn-2e-===Zn2+
B.电池反应为Zn+Cu2+===Zn2++Cu
C.在外电路中,电子从正极流向负极
D.取下盐桥,原电池仍可工作
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入铝粉能放出氢气的溶液中:CO32—、AlO2—、I—、NO3—
B.由水电离出的c(OH—)=10—13 mol·L—1的溶液中:Fe3+、NH4+、ClO—、Cl—
C.使pH试纸变红的溶液中:NH4+、Cu2+、SO42—、Cl—
D.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2—、Br—
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。下列说法正确的是
A.五种元素中原子半径最大的是E,最小的是A
B.A和B、D、E均能形成共价型化合物中,稳定性最差的是A、D形成的化合物
C.E最高价氧化物对应水化物化学式为H2EO4
D.C的单质在空气中燃烧产物的化学式为C2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关SO2说法中不正确的是
A.被酸雨污染的农田及湖泊可洒石灰石粉末;减轻其危害
B.在溶液BaCl2中通入SO2气体,溶液仍登清,滴入3%过氧化氢溶液有白色沉淀
C.能与水反应生成硫酸
D.二氧化硫能使品红溶液褪色,加热,品红溶液颜色恢复
查看答案和解析>>
科目:高中化学 来源: 题型:
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断
正确的是
A.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32-
B.含等物质的量的FeBr2、Fel2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com