
下列离子反应方程式正确的是( )
A.铜粉与98.3%的硫酸加热下反应:Cu+4H++SO ===Cu2++SO2↑+2H2O
===Cu2++SO2↑+2H2O
B.少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O―→C6H5 OH+HSO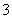
C.向氯化铝溶液中加入过量氨水:Al3++4NH3·H2O===AlO +2H2O+4NH
+2H2O+4NH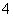
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2===2Fe3++2H2O
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
第119号未知元素,有人称为“类钫”。根据周期表结构及元素性质变化趋势,有关“类钫”的预测的说法错误的是
A.单质有较高的熔点 B.“类钫”在化合物中呈+1价
C.“类钫”具有放射性 D.“类钫”单质的密度小于1g.cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
用足量的CO还原13.7 g某铅氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0 g,则此铅氧化物的化学式是 ( )
A.PbO B.Pb2O3
C.Pb3O4 D.PbO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—化学与技术】
I.目前,我国采用“接触法”制硫酸,设备如图所示:
 (1)图中设备A的名称是_____________ ,该设备中主要反应的化学方程式为 。
(1)图中设备A的名称是_____________ ,该设备中主要反应的化学方程式为 。
(2)有关接触法制硫酸的下列说法中,不正确的是_______(填字
母序号)。
A.二氧化硫的接触氧化在接触室中发生
B.吸收塔用浓度为98.3%浓硫酸吸收三氧化硫
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失2%
D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
E.硫酸工业中在接触室安装热交换器是为了利用SO3转化为 H2SO4时放出的热量
II. 纯碱是一种重要的化工原料。制碱工业主要有“氨碱法”(索尔维法)和“联合制碱法”(侯氏制碱法)两种工艺。请按要求回答问题:
(3)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源于 ,“氨碱法”中CO2来源
于 。
(4)氨碱法的原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比) 。
(5)写出“联合制碱法”有关反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S。下列说法正确的是( )
A.反应中硫元素被氧化,所有铁元素均被还原
B.还原剂是S2-和Cu+,氧化剂是Fe3+
C.氧化产物是S,还原产物是Cu2+和Fe2+
D.当转移1 mol e-时,有46 g CuFeS2参加反应
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室欲配制一种仅含四种离子(不考虑来源于水电离的离子)的溶液,且溶液中四种离子的浓度均相等,能达到此目的的是( )
A.Na+、Mg2+、SO 、Cl- B.ClO-、I-、NH
、Cl- B.ClO-、I-、NH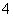 、Ba2+
、Ba2+
C.Na+、AlO 、K+、HCO
、K+、HCO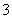 D.Al3+、K+、SO
D.Al3+、K+、SO 、NO
、NO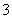
查看答案和解析>>
科目:高中化学 来源: 题型:
对于:2C4H10(g) + 13O2(g) = 8CO2(g) + 10H2O(l) △H=-5800kJ/mol 叙述错误的是( )
A.该反应的反应热为△H= -5800kJ/mol,是放热反应。
B.该反应的△H与各物质的状态有关,与化学计量数也有关。
C.该式的含义为:25℃、101kPa,2mol C4H10气体完全燃烧生成CO2和液态水时放出热量5800kJ。
D.由该反应的热化学方程式可知丁烷的燃烧热为5800kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com