
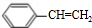 ,A分子中处于同一平面的原子最多有16个;
,A分子中处于同一平面的原子最多有16个;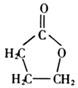 :
: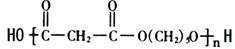 .
. 分析 现有A、B、C、D四种有机物,它们的相对分子质量都是104,其中A是芳香烃,则$\frac{104}{12}$=8…8,故A的分子式为C8H8,则A为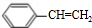 ,由nB→Y(聚酯)+nH2O,可知B分子中至少含有1个-COOH、1个-OH,结合相对分子质量可得,B只能含有1个-COOH,(2)中B也能发生分子内酯化生成五元环状化合物,则B分子至少含有4个碳原子,去掉1个-COOH、1个-OH剩余基团总式量为104-45-17=42,剩余基团为-C3H6-,分子内均没有甲基,则B为HOCH2CH2CH2COOH;由nC+nD→Z(聚酯)+2nH2O,应二元醇与二元羧酸反应,二元羧酸去掉2个-COOH剩余基团总式量为104-90=14,故羧酸为HOOCCH2COOH,二元醇去掉2个-OH剩余基团总式量为104-34=70,则$\frac{70}{14}$=5,分子中没有甲基,故二元醇为HOCH2CH2CH2CH2CH2OH,据此解答.
,由nB→Y(聚酯)+nH2O,可知B分子中至少含有1个-COOH、1个-OH,结合相对分子质量可得,B只能含有1个-COOH,(2)中B也能发生分子内酯化生成五元环状化合物,则B分子至少含有4个碳原子,去掉1个-COOH、1个-OH剩余基团总式量为104-45-17=42,剩余基团为-C3H6-,分子内均没有甲基,则B为HOCH2CH2CH2COOH;由nC+nD→Z(聚酯)+2nH2O,应二元醇与二元羧酸反应,二元羧酸去掉2个-COOH剩余基团总式量为104-90=14,故羧酸为HOOCCH2COOH,二元醇去掉2个-OH剩余基团总式量为104-34=70,则$\frac{70}{14}$=5,分子中没有甲基,故二元醇为HOCH2CH2CH2CH2CH2OH,据此解答.
解答 解:现有A、B、C、D四种有机物,它们的相对分子质量都是104,其中A是芳香烃,则$\frac{104}{12}$=8…8,故A的分子式为C8H8,则A为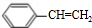 ,由nB→Y(聚酯)+nH2O,可知B分子中至少含有1个-COOH、1个-OH,结合相对分子质量可得,B只能含有1个-COOH,(2)中B也能发生分子内酯化生成五元环状化合物,则B分子至少含有4个碳原子,去掉1个-COOH、1个-OH剩余基团总式量为104-45-17=42,剩余基团为-C3H6-,分子内均没有甲基,则B为HOCH2CH2CH2COOH;由nC+nD→Z(聚酯)+2nH2O,应二元醇与二元羧酸反应,二元羧酸去掉2个-COOH剩余基团总式量为104-90=14,故羧酸为HOOCCH2COOH,二元醇去掉2个-OH剩余基团总式量为104-34=70,则$\frac{70}{14}$=5,分子中没有甲基,故二元醇为HOCH2CH2CH2CH2CH2OH.
,由nB→Y(聚酯)+nH2O,可知B分子中至少含有1个-COOH、1个-OH,结合相对分子质量可得,B只能含有1个-COOH,(2)中B也能发生分子内酯化生成五元环状化合物,则B分子至少含有4个碳原子,去掉1个-COOH、1个-OH剩余基团总式量为104-45-17=42,剩余基团为-C3H6-,分子内均没有甲基,则B为HOCH2CH2CH2COOH;由nC+nD→Z(聚酯)+2nH2O,应二元醇与二元羧酸反应,二元羧酸去掉2个-COOH剩余基团总式量为104-90=14,故羧酸为HOOCCH2COOH,二元醇去掉2个-OH剩余基团总式量为104-34=70,则$\frac{70}{14}$=5,分子中没有甲基,故二元醇为HOCH2CH2CH2CH2CH2OH.
(1)由上述分析可知,A的结构简式是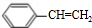 ,分子中苯环平面与乙烯平面可以共面,处于同一平面的原子最多有16个;
,分子中苯环平面与乙烯平面可以共面,处于同一平面的原子最多有16个;
故答案为: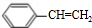 ;16;
;16;
(2)B为HOCH2CH2CH2COOH,发生分子内酯化生成五元环状化合物E为 ,
,
故答案为: ;
;
(3)HOOCCH2COOH与HOCH2CH2CH2CH2CH2OH发生缩聚反应得到高聚物Z为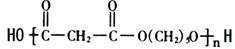 ,
,
故答案为: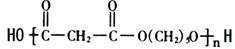 .
.
点评 本题考查有机物推断,根据发生的反应判断含有的官能团,注意利用商余法与残余法进行推断,题目具有一定猜测验证性,是对学生总部能力的考查,难度较大.


科目:高中化学 来源: 题型:解答题
 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
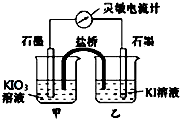 将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池.
将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物:是否含有共价键 | |
| B. | 氧化还原反应:元素化合价是否变化 | |
| C. | 强弱电解质:溶液的导电能力大小 | |
| D. | 溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
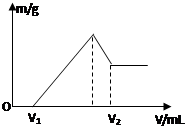 将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示.
将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝和干冰升华 | B. | 钠和硫熔化 | ||
| C. | 食盐和氯化氢溶解于水 | D. | 二氧化硅和二氧化硫熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含Ba(OH)2、KOH的混合溶液中缓慢通入CO2:Ba(OH)2、KOH、K2CO3、BaCO3 | |
| B. | 在含NH4+、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、NH4+、Al(OH)3 | |
| C. | 在含AlO2-、OH-、CO32-的溶液中逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入锌粉:Ag+、Cu2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
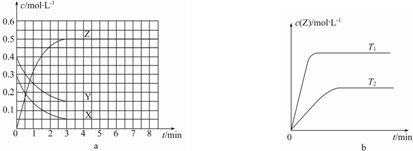
| A. | 该反应的正反应是放热反应 | |
| B. | 若在第6 min时升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| C. | 图a中反应达到平衡时,Y的转化率为37.5% | |
| D. | 反应中某时刻各物质的正反应速率为2v(X)═2v(Y)═v(Z) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
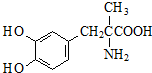
| A. | 分子式为C10H14NO4 | |
| B. | 分子中有一个手性碳原子 | |
| C. | 甲基多巴具有两性,且能发生酯化反应 | |
| D. | 1mol甲基多巴分子最多能与2 mol NaOH反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com