
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������������ȷ���ǣ�������
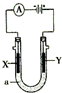
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������������ȷ���ǣ�������| A�� | ��X��YΪʯī��aΪ����NaCl��Һ����Y�����������̪����Y����Һ�ʺ�ɫ | |
| B�� | ��X��Y��ʯī��aΪAgNO3��Һ�����һ��ʱ�����Һ��pH��С | |
| C�� | ���õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ��X�缫�IJ����Ǵ�ͭ | |
| D�� | ��YΪ����XΪʯī��aΪϡ���ᣬY�缫��ӦΪFe-3e-=Fe3+ |
���� A����X��YΪʯī��aΪ����NaCl��Һ����X�缫�������������������������ƣ���Y�缫������������������
B����X��YΪʯī��aΪ��������Һ�����������ᡢ����������
C�����õ�ⷽ��������ͭ�����Һѡ��CuSO4��Һ�������Ǵ�ͭ�������Ǵ�ͭ��
D����YΪ����XΪʯī��������������������ʧ���ӷ���������Ӧ��
��� �⣺A����X��YΪʯī��aΪ����NaCl��Һ����X�缫�������������������������ƣ���Y�缫��������������������X�����������̪����X����Һ�ʺ�ɫ����A����
B����X��YΪʯī��aΪ��������Һ�����������ᡢ�������������һ��ʱ�����Һ��pH��С����B��ȷ��
C�����õ�ⷽ��������ͭ�����Һѡ��CuSO4��Һ�������Ǵ�ͭ�������Ǵ�ͭ����X�缫�IJ����Ǿ�ͭ����C����
D����YΪ����XΪʯī��������������������ʧ���ӷ���������Ӧ��Y�缫��ӦΪFe-2e-=Fe2+����D����
��ѡB��
���� ���⿼��ѧ�����صĹ���ԭ��֪ʶ����ͭ����ԭ�����������Ը�����ѧ֪ʶ���лش��ѶȲ���


 ��ս100��Ԫ����Ծ�ϵ�д�
��ս100��Ԫ����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Y
��Y ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ���� | B�� | �Ȼ�����Һ | C�� | ��������Һ | D�� | �Ȼ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
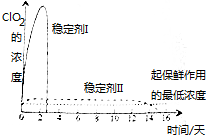 Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���
Ŀǰ���ȵ���������Cl2O��ClO2��Cl2O7�ȣ�����ClO2��Cl2���������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺���й����ݼ��±���| ��ѧʽ | Cl2O | ClO2 | Cl2O7 |
| �е�/�� | 3.8 | 11.0 | 82.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO32-+H2O?HCO3-+OH-�����ȵĴ�����Һ��ϴ���� | |
| B�� | Al3++3H2O?Al��OH��3+3H+����������ˮ | |
| C�� | Fe3++3H2O$\stackrel{��}{?}$Fe��OH��3�����壩+3H+ �Ʊ�Fe��OH��3���� | |
| D�� | SnCl2+H2O?Sn��OH��Cl��+HCl�����������Ȼ�������Һʱ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| �ӹ���Ӧ�� |  ��֬��Ӳ�� |  ������� |  ʯӢ������ź� |  Ư������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ��������м��Ӧ��2Fe+6H+=2Fe3++3H2 | |
| B�� | ��FeCl3��Һ�м�Mg��OH��2��3 Mg��OH��2+2Fe3+=2Fe��OH��3+3 Mg2+ | |
| C�� | NaHCO3��Һ��ϡH2SO4��Ӧ��CO32-+2H+=H2O+CO2�� | |
| D�� | ����CuSO4��Һ��Ӧ��2Na+Cu2+=Cu��+2Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
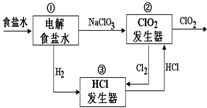 ����ʳ��ˮ��ȡClO2�Ĺ�ҵ��������ͼ��ʾ��
����ʳ��ˮ��ȡClO2�Ĺ�ҵ��������ͼ��ʾ��| A�� | װ�â���H2���������� | |
| B�� | װ�âڵ������缫��ӦʽΪ2ClO3-+12H++10e-=Cl2��+6H2O | |
| C�� | ��������Cl2��NaCl������ѭ������ | |
| D�� | Ϊ��ʹH2��ȫת��ΪHCl����Ҫ��װ�â��в���Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18 g H216O��20 g H218O���е���������Ϊ10NA | |
| B�� | 1L 1mol/L��KAl��SO4��2��Һ������������Ϊ2NA | |
| C�� | 0.2mol������������ϡ���ᷴӦ�����������ķ�����ĿΪ0.3NA | |
| D�� | ��ӦN2+3H2?2NH3��ƽ��ʱ��ÿ����3molH2ͬʱ��2NA��N-H���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com