
| A、纯水在25℃和80℃时的pH值 |
| B、25℃时,pH=3的盐酸和AlCl3溶液中,水电离的氢离子的浓度 |
| C、耐火材料CaO和MgO的熔点 |
| D、1L pH=2的盐酸和醋酸溶液中,分别投入足量锌粒,放出H2的物质的量 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、该溶液pH=4 |
| B、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
| C、此酸的电离平衡常数约为1×10-7 mol?L-1 |
| D、升高温度,溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤⑥ | B、③⑦ |
| C、⑤⑥⑦ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
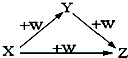 X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
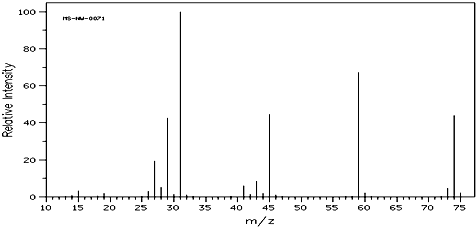
查看答案和解析>>
科目:高中化学 来源: 题型:
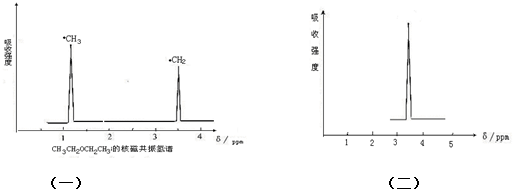
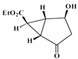
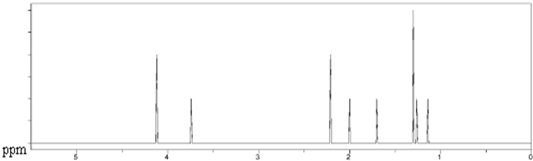
查看答案和解析>>
科目:高中化学 来源: 题型:
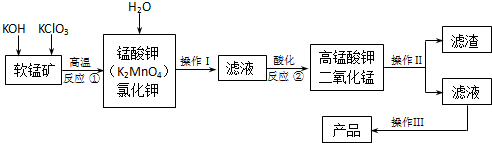
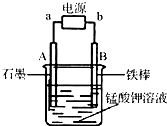
查看答案和解析>>
科目:高中化学 来源: 题型:
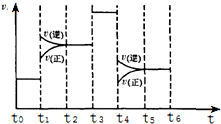 化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图是反应速率与时间的关系图,其中表示平衡混合物中CA3含量最高的一段时间是
化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),如图是反应速率与时间的关系图,其中表示平衡混合物中CA3含量最高的一段时间是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a可能为6 |
| B、a可能为5 |
| C、a可能为4 |
| D、a可能为3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com