
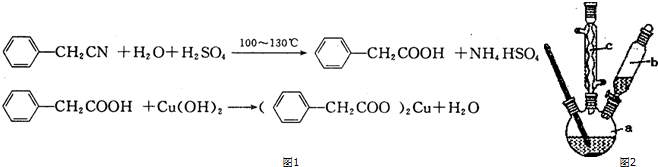
分析 (1)配制此硫酸时,应将密度大的注入密度小的液体中,防止混合时放出热使液滴飞溅;
(2)由图可知,c为冷凝管,使气化的液体冷凝回流,仪器b可加入反应液;
(3)反应结束后加适量冷水,降低温度,减小苯乙酸的溶解度;分离苯乙酸粗品,利用过滤操作;
(4)苯乙酸微溶于冷水,在水中的溶解度较小;由反应 +H2O+H2SO4 $\stackrel{100-130℃}{→}$
+H2O+H2SO4 $\stackrel{100-130℃}{→}$ +NH4HSO4可知,40g苯乙腈生成苯乙酸为40g×$\frac{136}{117}$=46.5g;
+NH4HSO4可知,40g苯乙腈生成苯乙酸为40g×$\frac{136}{117}$=46.5g;
(5)苯乙酸微溶于冷水,溶于乙醇,混合溶剂中乙醇可增大苯乙酸的溶解度.
解答 解:(1)稀释浓硫酸放出大量的热,配制此硫酸时,应将密度大的注入密度小的液体中,防止混合时放出热使液滴飞溅,则加入蒸馏水与浓硫酸的先后顺序是先加水、再加入浓硫酸,
故答案为:先加水、再加入浓硫酸;
(2)在实际操作时,发现b中液体不容易滴下来,可以改为恒压滴液漏斗或在滴加液体时打开上口活塞,由图可知,c为球形冷凝管,其作用为回流(或使气化的反应液冷凝),仪器b的作用为滴加苯乙腈;滴加苯乙腈,
故答案为:改为恒压滴液漏斗或在滴加液体时打开上口活塞;球形冷凝管;冷凝回流(或使气化的反应液冷凝);
(3)反应结束后加适量冷水,降低温度,减小苯乙酸的溶解度,则加入冷水可便于苯乙酸析出;分离苯乙酸粗品,利用过滤操作,则需要的仪器为漏斗、烧杯、玻璃棒,
故答案为:便于苯乙酸析出;BCE;
(4)苯乙酸微溶于冷水,在水中的溶解度较小,则提纯苯乙酸的方法是重结晶;由反应 +H2O+H2SO4 $\stackrel{100-130℃}{→}$
+H2O+H2SO4 $\stackrel{100-130℃}{→}$ +NH4HSO4可知,40g苯乙腈生成苯乙酸为40g×$\frac{136}{117}$=46.5g,最终得到44g纯品,则苯乙酸的产率是$\frac{44g}{46.5g}$×100%=94.6%,
+NH4HSO4可知,40g苯乙腈生成苯乙酸为40g×$\frac{136}{117}$=46.5g,最终得到44g纯品,则苯乙酸的产率是$\frac{44g}{46.5g}$×100%=94.6%,
故答案为:重结晶;94.6;
(5)苯乙酸微溶于冷水,溶于乙醇,混合溶剂中乙醇可增大苯乙酸的溶解度,然后与Cu(OH)2反应除去苯乙酸,即混合溶剂中乙醇的作用是增大苯乙酸溶解度,便于充分反应,
故答案为:增大苯乙酸溶解度,便于充分反应.
点评 本题考查苯乙酸铜的合成,侧重物质制备实验及有机物性质的考查,把握合成反应及实验装置的作用为解答的关键,综合考查学生实验技能和分析解答问题的能力,题目难度中等,注意信息的处理及应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ②③④ | C. | ②③⑤ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
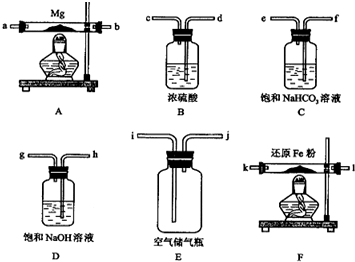
| 装置 | 目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
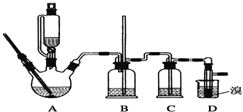
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用物质A表示2 s内的平均反应速率为0.3 mol/(L•s) | |
| B. | 用物质B表示2s内的平均反应速率为0.6 mol/(L•s) | |
| C. | 2 s后物质B的浓度为0.35 mol/L | |
| D. | 2 s后物质A的转化率为30% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com