
【题目】亚硝酸钠是一种工业盐,虽然和食盐很像,但有毒,不能食用。以下为亚硝酸钠的工业生产流程:
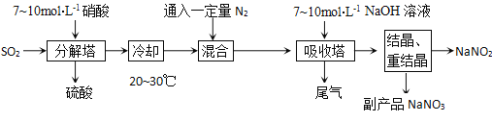
(1)首先在反应塔中通SO2和淋入硝酸,控制反应生成的NO与NO2物质的量之比恰好1:1,则分解塔中发生反应的化学方程式为: 。试从产物产率的角度分析该反应中硝酸的浓度不宜过大或过小的原因是 。
(2)吸收塔中所发生化学反应方程式为: 。
(3)为测定亚硝酸钠的含量,称取4.500 g样品溶于水配成250 mL溶液,取20.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:

①锥形瓶中发生反应的离子方程式为 。
②第一组实验数据出现异常,造成这种异常的原因可能是_________(填代号)。
A.酸式滴定管用蒸馏水洗净后用标准液润洗
B.滴定终点时仰视读数
C.锥形瓶洗净后未干燥
③根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
【答案】
(1)2HNO3 + 2SO2 + H2O ═ NO+ NO2+ 2H2SO4;硝酸浓度过大,主要还原生成NO2,导致亚硝酸钠产率降低;若硝酸浓度过低,分解塔中出来的主要是NO,亚硝酸钠产率也低;
(2)NO + NO2 + 2NaOH ═ 2NaNO2 + H2O;
(3)①5NO2- + 2MnO4-+ 6H+ = 5NO3-+ 2Mn2++ 3H2O;②b ;③95.83%
【解析】
试题分析:(1)HNO3被还原后生成的NO与NO2物质的量之比恰好是1:1,即2molHNO3被还原时氮元素得4mol电子,能将2molSO2氧化为2molH2SO4,故化学方程式为:2HNO3+2SO2+H2O═NO+NO2+2H2SO4;浓硝酸的还原产物是NO2,稀硝酸的还原产物是NO,故当硝酸浓度过大,主要还原生成NO2,导致亚硝酸钠产率降低;若硝酸浓度过低,分解塔中出来的主要是NO,亚硝酸钠产率也低,故答案为:2HNO3+2SO2+H2O═NO+NO2+2H2SO4;硝酸浓度过大,主要还原生成NO2,导致亚硝酸钠产率降低;若硝酸浓度过低,分解塔中出来的主要是NO,亚硝酸钠产率也低;
(2)一氧化氮和二氧化氮被氢氧化钠溶液吸收,反应的方程式为NO + NO2 + 2NaOH ═ 2NaNO2 + H2O,故答案为:NO + NO2 + 2NaOH ═ 2NaNO2 + H2O;
(3)①锥形瓶中亚硝酸钠和高锰酸钾发生氧化还原反应,反应的离子方程式为5NO2- + 2MnO4-+ 6H+ = 5NO3-+ 2Mn2++ 3H2O,故答案为:5NO2- + 2MnO4-+ 6H+ = 5NO3-+ 2Mn2++ 3H2O;
②第一组实验数据消耗的酸性高锰酸钾溶液体积偏大,会导致测量结果偏高。a.酸式滴定管用蒸馏水洗净后用标准液润洗,对实验无影响,故a错误;b.滴定终了仰视读数,导致读数偏大,计算出的标准液体积偏大,故b正确;c.锥形瓶不需要干燥,所以锥形瓶洗净后未干燥,不影响测定结果,故c错误;故答案为:b;
③由于第一组数据偏高,应该舍弃;其它三组消耗标准液平均体积为:![]() mL=20.00mL,25mL样品消耗高锰酸钾的物质的量为0.1000mol/L×0.02L=0.002mol,则250mL样品溶液会消耗高锰酸钾的物质的量为0.002mol×
mL=20.00mL,25mL样品消耗高锰酸钾的物质的量为0.1000mol/L×0.02L=0.002mol,则250mL样品溶液会消耗高锰酸钾的物质的量为0.002mol×![]() =0.025mol,根据化合价变化可得反应关系式:2MnO4-~5NO2-,则4.000g样品中含有亚硝酸钠的物质的量为0.025mol×
=0.025mol,根据化合价变化可得反应关系式:2MnO4-~5NO2-,则4.000g样品中含有亚硝酸钠的物质的量为0.025mol×![]() =0.0625mol,质量为69g/mol×0.0625mol=4.3125g,所以反应后的固体中亚硝酸钠的质量分数为:
=0.0625mol,质量为69g/mol×0.0625mol=4.3125g,所以反应后的固体中亚硝酸钠的质量分数为:![]() ×100%=95.8%,故答案为:95.8%。
×100%=95.8%,故答案为:95.8%。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)光束通过Fe(OH)3胶体,可看到光亮的通路,这种现象叫________;
(2)19g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,求ACl2的摩尔质量________
(3)在标准状况下,测得4.2g气体A的体积是3360mL,则A可能是什么气体________
(4)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的体积之比是________。
(5)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。所得盐酸物质的量浓度分别是________
(6)现有以下物质:①NaCl晶体 ②盐酸 ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧浓H2SO4 ⑨KOH固体;以上物质中属于电解质的是________
(7)Ca(HCO3)2溶液与少量氢氧化钠溶液混合的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一种重要化工生产的中间体,已知其结构简式如下图:
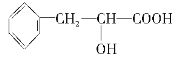
(1)A中含有的含氧官能团的名称
(2)A可能具有的化学性质有 (填写序号)。
①能与H2发生加成反应
②一定条件下可发生缩聚反应
③能与甲酸发生酯化反应
④能在浓硫酸和加热的条件下发生消去反应
⑤能与Ag(NH3)2OH溶液发生氧化反应
(3)A的一种同分异构体B,与Ag(NH3)2OH溶液混合于试管中水浴加热有银镜产生;B与浓溴水发生苯环上的取代反应时,1mol B能与3mol Br2恰好反应。请写出B发生银镜反应的化学方程式:
(只要求写出一个化学方程式,有机物写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
A | 1mol | 2NA | |
B | 22.4L | 1mol | |
C | 106g | 1mol | |
D | 106g | 2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的沸点由高到低排列的是
①CH3(CH2)2CH3
②CH3(CH2)3CH3
③(CH3)3CH
④(CH3)2CHCH2CH3.
A. ④②①③
B. ②④①③
C. ④①②③
D. ②④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的M层上的电子数比K层多5。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第 周期 族; ]
(2) C的离子结构示意图是 ,F中的化学键为 ;
(3) AB2的电子式为 ; F和AB2反应的化学方程式为 ;
(4) C、D、E三种元素的原子半径从小到大的顺序为 ; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法不正确的是( )
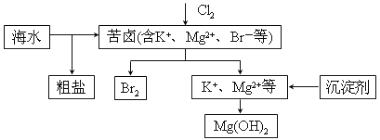
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
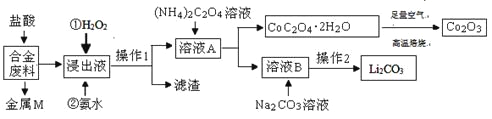
(1)金属M为__________。
(2)加入H2O2的作用是(用离子方程式表示)____________,加入氨水的作用是________。
(3)CoC2O4﹒2H2O高温焙烧的化学方程式为__________________________。
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其目的是___________,90℃时Ksp(Li2CO3)的值为___________。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL-1 | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com