
| 1 |
| 2 |
| n |
| V |
| 1 |
| 2 |
| a |
| 2 |
| a |
| 2 |
| (2b-a)mol | ||
|
| 2(2b-a) |
| V |
| 2(2b-a) |
| V |
| 2(2b-a) |
| V |


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
| A、只有④ | B、有④⑤ |
| C、有②④⑤ | D、全部都对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、铝片碱洗时常有气泡:2Al+2OH-+2H2O═2AlO
| ||
B、Al2O3溶于氨水:Al2O3+2OH-═2AlO
| ||
C、AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO
| ||
D、实验室用铝盐制Al(OH)3:Al3++3NH3?H2O═Al(OH)3↓+3NH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1173 kJ |
| B、1456 kJ |
| C、2022 kJ |
| D、2346 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6 g |
| B、11.2 g |
| C、22.4 g |
| D、33.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:

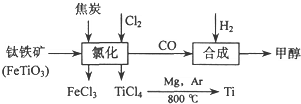
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3O4可写成FeO?Fe2O3,Pb3O4也可写成PbO?Pb2O3 |
| B、NaCl与HCl化学式相似,故NaCl与HCl的结构也相似 |
| C、由“2Fe+3Cl2═2FeCl3”反应可推出“2Fe+3I2═2FeI3”反应也能发生 |
| D、金属镁失火不能用CO2灭火;金属钠失火也不能用CO2灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com