
【题目】摩尔质量是 ______ 的物质所具有的质量![]() 符号: ______
符号: ______ ![]() 单位: ______ 或 ______ .
单位: ______ 或 ______ .
A. 单位物质的量;M;![]() ;
;![]()
B. 物质的量;m;![]() ;
;![]()
C. 单位物质的量;m;g;![]()
D. 物质的量;M;![]() ;kg
;kg
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】实验室配制460mL0.1mol/LNaOH溶液,回答下列问题:
(1)完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、_____、_____等。
(2)应用托盘天平称取NaOH固体的质量为_________。
(3)下面操作造成所配NaOH溶液浓度偏高的是_________________
A .将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
B .摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C .定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E. NaOH固体放在烧杯中称量时间过长
(4)取上述体积均为150mL的 A、B 两份NaOH 溶液,分别通入一定量的 CO2 后,再向所得溶液中滴加一定物质的量浓度的盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
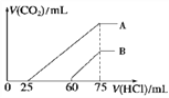
①B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
②A 曲线表明,盐酸的浓度为______mol/L;通入的CO2在标准状况下的体积为______mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列事实中,什么因素影响了化学反应的速率?
(1)食品容易霉变,冬天就不容易发生该现象;
(2)氯酸钾放出气泡很慢,撒入少量二氧化锰很快产生气体 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列有机物:
① CH2=CH2 ②![]()
③ CH3CH(OH)CH2CH3 ④ (CH3)2C=CH2
⑤ CH3CH2OCH2CH3 ⑥ CH3CH=CHCH=CHCOOH
(1)属于羧酸的是_____(填序号)。
(2)与③互为同分异构体的是_____(填序号)。
(3)与①互为同系物的是_____(填序号)。
(4)用系统命名法给④命名,其名称为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校同学在实验室中对一氧化碳与硫酸钙反应进行了探究。回答下列问题:
(1)甲组同学利用CaSO4·2H2O在400--500℃脱水制取无水CaSO4。实验中需用到的加热装置中的硅酸盐质的仪器除玻璃棒外,还用到______________。
(2)乙组同学利用H2C2O4·2H2O在浓硫酸作用下脱水生成CO、CO2并制备纯净的CO气体,实验装置如下:
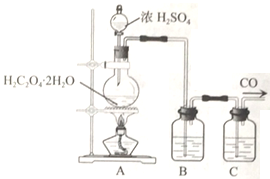
B、C中盛放的试剂依次为______、____________。
(3)丙组同学利用甲组制得的无水CaSO4和乙组制得的CO并利用下列装置验证反应并检验气态产物中有SO2和CO2产生。
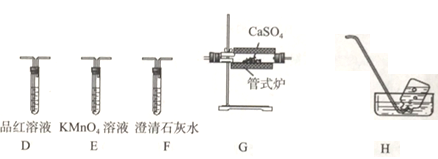
①上述装置(部分装置可重复使用)的连接顺序为C→___________。
②若E溶液褪色,则发生反应的离子方程式为_____________。
③能证明有CO2的生成的实验依据是____________。
④若G中产物为CaO,则G中发生反应的化学方程式为_________________。
(4)丁组的同学取丙组实验后G装置中的固体产物加入试管中,然后加人足量稀盐酸,固体完全溶液且产生少量气体,通入CuSO4溶液有黑色沉淀。可验证CO与CaSO4在高温下还发生了一个副反应,该反应为______________(用方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是几种常见有机物之间的转化关系,下列有关说法正确的是( )
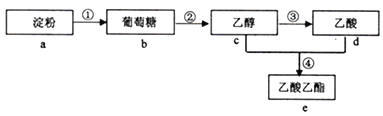
A. 反应①、②、③、④均属于取代反应
B. 反应④的条件为:稀硫酸,加热
C. 与d含有相同官能团的e的同分异构体只有1种
D. a遇碘单质变蓝,b能与银氨溶液水浴加热条件下反应析出银
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,工业大规模生产前,实验室先按如下流程进行模拟制备少量Mg(ClO3)2·6H2O:
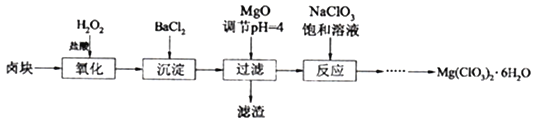
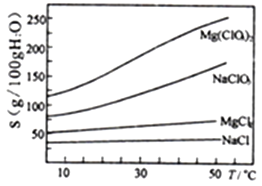
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②几种化合物的溶解度(S)随温度(T)变化曲线如右图。
(1)卤块中加H2O2的目的是________________,写出该反应的离子方程式__________________。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全?_________________。
(3)常温下,加MgO调节pH=4后溶液中c(Fe3+)=___________(已知Ksp[Fe(OH)3=4×10-38],过滤所得滤渣的主要成分有______________。
(4)加入NaClO3饱和溶液公有NaCl晶体析出,写出该反应的化学方程式:___________,请利用该反应,结合上图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应;②蒸发结晶;③___________;④冷却结晶;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol;
(2)该气体所含原子总数为____________个;
(3)该气体在标准状况下的体积为____________L;
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为_____________;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为____________mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com