
| ||
| ||


科目:高中化学 来源: 题型:
| A、分散质的粒子都可以通过滤纸 |
| B、胶体是介稳定的,所以Fe(OH)3 胶体密封一段时间也会产生沉淀 |
| C、都能产生丁达尔效应 |
| D、加入盐酸先产生沉淀,然后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 顺序 | 编号 | 反应现象 |
| ① | A+B | 有无色气体逸出 |
| ② | A+C | 没有现象 |
| ③ | B+D | 有无色气体逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
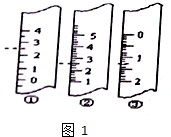 中用水稀释后转移到100mL容量瓶中定容,然后将稀释后的溶液倒入试剂瓶中.
中用水稀释后转移到100mL容量瓶中定容,然后将稀释后的溶液倒入试剂瓶中.
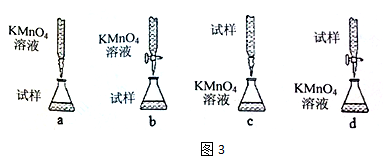
| 实验序号 | 待测样品溶液的体积/mL | 0.1000mol.L-1 KMnO4溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 24.98 |
| 2 | 25.00 | 1.56 | 29.30 |
| 3 | 25.00 | 1.00 | 26.02 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com