
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质量数不同,属于两种元素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、H2互为同位素 | |
| C. | 14462Sm其原子核内中子数和质子数都是62 | |
| D. | O2和O3互为同素异形体 |
分析 A.质子数相同的原子属于同种元素;
B.同位素的研究对象是原子;
C.中子数=质量数-质子数;
D.同种元素的不同单质互称同素异形体.
解答 解:A.质子数相同的原子属于同种元素,${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质子数相同,属于同种元素,故A错误;
B.同位素的研究对象是原子,${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、互为同位素,H2为分子,故B错误;
C.14462Sm其原子核内质子数为62,质量数为144,则中子数为144-62=82,所以中子数和质子数不同,故C错误;
D.同种元素的不同单质互称同素异形体,则O2和O3互为同素异形体,故D正确.
故选D.
点评 本题考查元素、同位素、同素异形体的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.


科目:高中化学 来源: 题型:选择题
| A. | 用Na与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 少量Ca(HCO3)2溶液与NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 石灰石溶于稀盐酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 铁与硫酸铜溶液反应:2Fe+3Cu2+═2Fe3++3Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ | |
| B. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ | |
| C. | 0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度30℃ | |
| D. | 0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CCl4的分子数约为NA个 | |
| B. | 常温常压下,3.2gO2和O3混合气体中含有的氧原子数目为0.2NA | |
| C. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA | |
| D. | 高温高压下,28gN2与6gH2反应,生成的NH3分子数为2nA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L甲烷气体含有的甲烷分子数为0.5NA | |
| B. | 标准状况下,22.4 L氦气与22.4 L氮气所含原子数相同 | |
| C. | 标准状况下,11.2 L CO与N2的混合气体与11.2 L O2所含分子数相同,原子数也相同 | |
| D. | 标准状况下,22.4 L CCl4中含共价键数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
| 第一次实验 | 第二次实验 | |
| 坩埚质量(g) | 14.520 | 14.670 |
| 坩埚质量+晶体质量(g) | 17.020 | 18.350 |
| 第一次加热、冷却、称量(g) | 16.070 | 16.989 |
| 第二次加热、冷却、称量(g) | 16.070 | 16.988 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
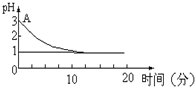 关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点:
关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CO+O2═2CO2 | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | 2KClO3═2KCl+3O2↑ | D. | Fe2O3+3CO═2Fe+3CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com