
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。请回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用____________形象化描述。在基态14C原子中,核外存在___________对自旋相反的电子。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为__________________________。
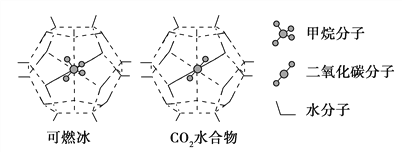
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
①下列关于CH4和CO2的说法正确的是________(填序号)。
a.CO2分子中含有2个σ键和2个π键
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0. 586 nm,根据上述图表所提供的数据分析,提出该设想的依据是______________________________________。
【答案】 电子云 2 H、C、O ad CO2的分子直径小于笼状空腔直径,且与H2O的结合力大于CH4
【解析】试题分析:本题考查电子云的概念、电负性的比较、σ键和π键的判断、杂化方式的判断、熔点高低的比较等。
(1)处于一定空间运动状态的电子在原子核外出现的概念密度分布可用电子云形象化描述。基态14C原子的轨道表示式为![]() ,核外存在2对自旋相反的电子。
,核外存在2对自旋相反的电子。
(2)CH4中C为-4价,H为+1价,电负性:C![]() H;非金属性:O
H;非金属性:O![]() C,电负性:O
C,电负性:O![]() C;C、H、O三种元素电负性由小到大的顺序为:H
C;C、H、O三种元素电负性由小到大的顺序为:H![]() C
C![]() O。
O。
(3)①a项,CO2的结构式为O=C=O,CO2分子中含有2个σ键和2个π键,a项正确;b项,CH4分子中含极性共价键,由于CH4为正四面体结构,CH4分子中正电中心和负电中心重合,CH4为非极性分子,b项错误;c项,CH4的相对分子质量小于CO2的相对分子质量,CH4分子间作用力小于CO2分子间作用力,CH4的熔点低于CO2,c项错误;d项,CH4中碳原子采取sp3杂化,CO2中碳原子采取sp杂化,d项正确;答案选ad。
②根据表中数据,CO2的分子直径(0.512nm)小于笼状结构的空腔直径(0.586nm),CO2与H2O的结合能(29.91kJ/mol)大于CH4与H2O的结合能(16.40kJ/mol),所以可用CO2置换“可燃冰”中的CH4。


科目:高中化学 来源: 题型:
【题目】在恒温恒容密闭容器中发生反应NH2COONH4(s)2NH3(g)+CO2(g),不能判断该反应已达到化学平衡的是( )
A. v正(NH3)=2v逆(CO2) B. 密闭容器中混合气体的平均摩尔质量不变
C. 密闭容器中混合气体的密度不变 D. 密闭容器中总压强不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
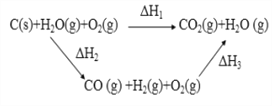
A. ΔH1=ΔH2+ΔH3
B. ΔH1<0 、 ΔH2>0 、 ΔH3<0
C. 将煤转化为 H2(g) 和 CO(g)后燃烧比煤直接燃烧放出热量多
D. 将煤转化为水煤气后再燃烧,从提高煤燃烧利用率看是得不偿失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.胶体能产生丁达尔效应
C.胶体分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,C为原子核内有12个中子的二价金属,当2.4gC与足量热水反应时,在标准状况下放出气体2.24L,D的M层上7个电子。
(1)写出A的离子结构示意图:___________,B在周期表的位置:______________,写出C的元素符号________,D的最高价氧化物化学式_______。
(2)比较D的气态氢化物与H2S和HF的稳定性:______>_______>______
(3)C与D两元素最高价氧化物的水化物发生化学反应的离子方程式______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定体积 CaCl2 和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1 的 Na2CO3溶液,反应过程中加入的 Na2CO3 溶液的体积与产生沉淀或气体的质量关系如图所示。
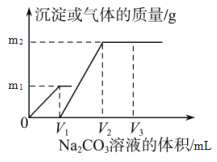
已知:图中 V1: V2=1:2,当加入 V2mLNa2CO3 溶液时,所得溶液的浓度为 1.00 mol·L-1,体积为 200mL。求:
(1)混合溶液中 CaCl2和 HCl 物质的量之比n(CaCl2)∶n(HCl)=_______。
(2)m2=______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
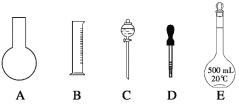
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 ____________________。
(2)在容量瓶的使用方法中,下列操作不正确的是____________。
A.使用容量瓶前检验是否漏水。
B.容量瓶用水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的质量为_______g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度______0.1mol/L(填“大于”“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.10 mol/L甲胺的溶液中滴加0.10 mol/L盐酸时混合溶液的pH与相关微粒的浓度关系如图所示。已知:甲胺(CH3NH2)类似于氨,但碱性稍强于氨。下列说法不正确的是

A. 甲胺在水中的电离方程式CH3NH2+H2O![]() CH3NH3++OH—
CH3NH3++OH—
B. b点对应的加入盐酸的体积小于20mL
C. 将等物质的量的CH3NH2和CH3NH3Cl一起溶于蒸馏水,得到对应a点的溶液
D. 常温下,甲胺的电离常数为Kb,则pKb=—lgKb=3.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
三位分别来自瑞士、美国、英国的科学家因发展“冷冻电子显微镜技术对溶液中的生物分子进行高分辨率结构测定”所做出的贡献而获得2017年诺贝尔化学奖。含有有机杂化锌、锗以及砷等金属的硒化物具有离子交换、催化、吸附、半导体等性能,显示出良好的应用前景。回答下列问题:
(1)锌基态原子核外电子排布式为_________。位于元素周期表五个分区中的________区。
(2)元素锗与砷中,第一电离能较大的是________ (填元素符号,下同),基态原子核外未成对电子数较少的是________。
(3)元素砷与氮同主族,二者的氢化物中熔沸点较高的是_________,原因是________。
(4)H2SeO3分子中Se 原子的杂化形式为________,H2SeO4的酸性比H2SeO3强,原因是________ 。
(5)气态SeO3分子的立体构型为______,与SeO3互为等电子体的一种离子为_____(填离子符号)。
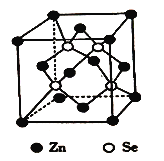
(6)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_____,若该晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏伽德罗常数的数值,则晶胞参数α为_____nm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com