
科目:高中化学 来源: 题型:
(1)氢是未来最好的能源选择,制取氢气的成熟的方法有很多,利用甲醇可以与水蒸气反应生成氢气,反应方程式如下:
CH3OH(g) + H2O(g) CO2(g) + 3H2(g)
CO2(g) + 3H2(g)  H(298K)=+ 49.4 kJ/mol
H(298K)=+ 49.4 kJ/mol
一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的 倍。
②该条件下的该反应的平衡常数是 (结果保留两位有效数字)。
③该条件下反应达平衡状态的依据是(填序号) 。
A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2) 甲、乙两容器体积相等,甲容器通入1 mol SO2和1 mol O2,乙容器通入1 mol SO3和0.5 mol O2,发生反应:2SO2(g) + O2 (g)  2SO3(g)
2SO3(g)  H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b 1(填“﹤”、“﹥”或“=”) 。
H<0,甲、乙起始反应温度相同,均和外界无热量交换,平衡时,甲中SO2的转化率为a,乙中SO3的分解率为b,则a、b的关系为a+b 1(填“﹤”、“﹥”或“=”) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,溶质的物质的量浓度为1 mol/L的是( )
A.将40 g NaOH溶于1 L水所得的溶液
B.将80 g SO3溶于水并配成1 L的溶液
C.将0.5 mol/L的NaNO3溶液100 mL加 热蒸发掉50 g水的溶液
热蒸发掉50 g水的溶液
D.含K+为2 mol的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在杠杆的两端分别挂着质量和体积都相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图所示,则下列说法正确的是( )
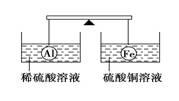
A、铝球一定是空心的
B、左边烧杯中的溶液质量减少了
C、去掉两烧杯杠杆仍平衡
D、右边铁球上出现红色
查看答案和解析>>
科目:高中化学 来源: 题型:
在Fe(OH)3胶体中,逐滴加入HI稀溶液,会出现一系列变化。
(1)先出现红褐色沉淀,原因是______________________________________。
(2)随后沉淀溶解,溶液呈黄色,此反应的离子方程式是________________________
________________________________________________________________________。
(3)最后溶液颜色加深,原因是________,此反应的离子方程式是_______________________________________ _________________________________。
_________________________________。
(4)若用稀盐酸代替HI稀溶液,能出现上述哪些相同的现象(填写上面各题序号)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液组成的描述合理的是( )
A.无色溶液中可能大量存在Al3+、NH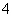 、Cl-、S2-
、Cl-、S2-
B.酸性溶液中可能大量存在Na+、ClO-、SO 、I-
、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
某离子反应中涉及H2O、ClO-、NH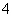 、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图K61所示。下列判断正确的是( )
、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图K61所示。下列判断正确的是( )
A.该反应中的还原剂是Cl-
B.每消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2∶3
D.反应后溶液的酸性明显增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com