
某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
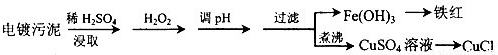
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是____________.调pH的最适宜范围为_______________
(2) 调PH过程中加入的试剂最好是_________
A.NaOH B.CuO C.NH3 ﹒H2O D.Cu2(OH)2CO3
(3)煮沸CuSO4溶液的原因是_____________________。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式________________。
(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是_________________。
(5) 称取所制备的CuCl样品0.250 0 g置于一定量的0.5 mol﹒L-1FeCl3溶液中,待样品完全溶解后,加水20 mL,用0.1000 mol﹒L-1的Ce((SO4)2溶液滴定,到达终点时消耗Ce((SO4)2溶液25.00 mL。有关的化学反应为 Fe3++CuCl=Fe2++Cu2++Cl-, Ce4++Fe2+=Fe3++Ce3+。计算该CuCl样品的质量分数_______________。
科目:高中化学 来源:2017届江西省高三上第二次段考化学卷(解析版) 题型:选择题
下列说法不正确的是
A.光导纤维、硝化纤维、铜氨纤维、玻璃纤维的主成分都是糖类
B.生理盐水、葡萄糖注射液都不能产生丁达尔效应现象,不属于胶体
C.红外光谱仪可用于测定化合物的官能团、 1H核磁共振仪可确定H所处的化学环境
D.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可到达水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学卷(解析版) 题型:选择题
下列各项操作错误的是
A.萃取、分液前需对分液漏斗检漏
B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出
C.为保证分液漏斗内的液体顺利流出,需将分液漏斗上面的塞子打开
D.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
有机结构理论中有一个重要的观点:有机化合物分子中,原子(团)之间相互影响,从而导致有机化合物化学性质不同。以下事实中,不能够说明此观点的是 ( )
A. 乙烯能使酸性KMnO4溶液退色,而甲烷不能
B. 甲苯能使酸性KMnO4溶液退色,而甲烷不能
C. 乙酸能与NaHCO3反应放出气体,而乙醇不能
D. 苯硝化反应一般生成硝基苯,而甲苯硝化反应生成三硝基甲苯
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
1 mol  分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 ( )
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 ( )
A.1mol、2mol B.2mol、3mol C.3mol、2mol D.3mol、3mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上阶段测二化学卷(解析版) 题型:选择题
下表是五种银盐的浓度积常数(25℃),下列有关说法错误的是
化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
A.将AgCl溶解于水后,向其中加入Na2S,则可以生成黑色的Ag2S沉淀,反应方程式为Ag+ + S2- = Ag2S↓
B.向AgCl沉淀中继续加入一定量的水,溶液中溶解的Ag+浓度不变
C.向含有0.1mol/LCl-,Br-,I-的溶液中加入逐渐加入硝酸银溶液,先生成的是黄色的AgI
D.常温下,AgCl、AgBr和Ag2SO4三种物质的溶解度逐渐减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上阶段测二化学卷(解析版) 题型:选择题
下列有关溶液中离子存在和转化的表达合理的是
A.向0.lmol/L、pH=l的NaHA 溶液中加入 NaOH 溶液:HA-+OH-=A2-+H2O
B.标准状况下,将1.12LCO2气体通入lL0.lmol/L的NaA1O2溶液中:
CO2+2H2O+A1O2-=A1(OH)3↓+HCO3-
C.由水电离出的c(H+)=1×1012mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3-
D.向NH4A1(SO4)2溶液中滴加 Ba(OH)2溶液使 SO42-完全沉淀:
NH4++Al3++2SO42-+2Ba2++4OH-=NH3·H2O+Al(OH)3↓+2BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考二化学试卷(解析版) 题型:选择题
25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511KJ/mol,下列说法正确的是( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s) △H=-317kJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期12月月考化学卷(解析版) 题型:选择题
现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下明所示,下列说法正确的是

A.该溶液中能确定存在的离子是Ba2+、AlO2-、NH4+
B.肯定不存在的离子是SO42-、OH-
C.若不能确定的离子中至少还存在着一种阳离子,则该离子的最小浓度为0.2 mol/L
D.OA段反应的离子方程式:2 AlO2-+ CO2+3H2O=2Al(OH)3↓+CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com