
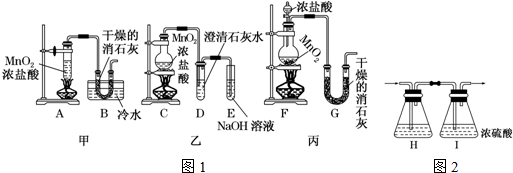
分析 (1)依据题意可知:用Cl2和Ca(OH)2制漂白粉的反应是放热反应,温度稍高时发生副反应:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O,结合氯气有毒,不进行尾气处理容易造成环境污染解答;
(2)合理装置应分三部分:制备氯气、氯气与氢氧化钙反应制取漂白粉、尾气处理装置,据此解答;
(3)浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢能够与氢氧化钙反应生成氯化钙和水,降低产率;
氯气与Ca(OH)2反应也会生成水,没必要干燥,洗气瓶Ⅰ多余.
解答 解:(1)依据题意可知:用Cl2和Ca(OH)2制漂白粉的反应是放热反应,温度稍高时发生副反应:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O,结合氯气有毒,不进行尾气处理容易造成环境污染,所以丙装置缺点:容易造成污染,容易发生副反应;
故答案为:容易造成污染,容易发生副反应;
(2)合理装置应分三部分:制备氯气、氯气与氢氧化钙反应制取漂白粉、尾气处理装置,制备装置中:A不加热不能得到氯气,C中不能控制氯气的产生速率,所以应选择F;
氯气与氢氧化钙反应温度稍高时发生副反应,所以应采取降温措施,应选择装置B;
氯气有毒需要进行尾气处理,应选择装置E;
正确的顺序为:FBE;
故答案为:FBE;
(3)浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢能够与氢氧化钙反应生成氯化钙和水,方程式:2HCl+Ca(OH)2═CaCl2+H2O;HCl消耗了Ca(OH)2,降低产率;
氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,所以应在前两个仪器之间应增加如图2所示装置盛有饱和食盐水,除去氯气中的氯化氢气体;
氯气与Ca(OH)2反应也会生成水,没必要干燥,洗气瓶Ⅰ多余;
故答案为:饱和氯化钠溶液;除去氯气中混有的氯化氢气体;
2HCl+Ca(OH)2═CaCl2+H2O;HCl消耗了Ca(OH)2,降低产率;
无;氯气与Ca(OH)2反应也会生成水,没必要干燥;
点评 本题以氯化钙的制备为载体考查了氯气的实验室制备、实验装置的选择和评价,题目难度不大,注意实验设计的严密性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | Na2SO3固体、浓H2SO4 | SO2 | |
| Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
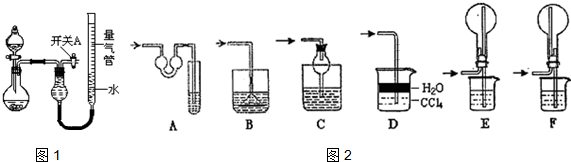
| 编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
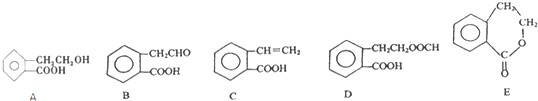
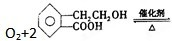 2
2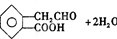
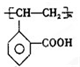
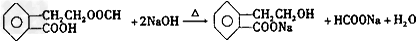 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
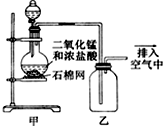
| A. | 该装置图中至少存在两处明显错误 | |
| B. | 烧瓶中的MnO2可换成KClO3或KMnO4 | |
| C. | 在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出 | |
| D. | 在乙后连一盛有饱和食盐水的烧杯可进行尾气处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- | |
| C. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com