
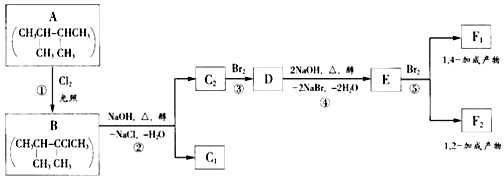
分析 由转化关系可知,A在光照条件下与氯气发生取代反应生成B,B在氢氧化钠醇溶液、加热条件下发生消去反应生成C1、C2,C2与溴发生加成反应生成D,D在氢氧化钠醇溶液、加热条件下发生消去反应生成E,E与溴可以发生1,2-加成反应生成F2,发生1,4-加成反应生成F1,则E为CH2=C(CH3)C(CH3)=CH2、F2为CH2=C(CH3)CBr(CH3)CH2Br,F1为BrCH2C(CH3)=C(CH3)CH2Br,结合逆合成法可得D为CH3CBr(CH3)CBr(CH3)2,C2为(CH3)2C=C(CH3)2,C1为(CH3)2CHC(CH3)=CH2,以此来解答.
解答 解:(1)上述框图中,反应①为烷烃光照下发生取代反应,则反应类型为取代反应,故答案为:取代;
(2)D为CH3CBr(CH3)CBr(CH3)2,E为CH2=C(CH3)C(CH3)=CH2,D生成E的化学方程式为CH3CBr(CH3)CBr(CH3)2+2NaOH$→_{△}^{醇}$CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O,
故答案为:CH3CBr(CH3)CBr(CH3)2+2NaOH$→_{△}^{醇}$CH2=C(CH3)C(CH3)=CH2+2NaBr+2H2O;
(3)由上述分析可知,C1的结构简式为(CH3)2CHC(CH3)=CH2,故答案为:(CH3)2CHC(CH3)=CH2.
点评 本题考查有机物的推断,为高频考点,把握转化中反应条件、官能团与性质、有机反应为解答的关键,侧重分析与推断能力的考查,注意卤代烃、烯烃性质的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH4+2 O2$→_{△}^{催化剂}$CO2+2H2O | B. | 2CH2=CH2+O2$→_{△}^{催化剂}$2CH3CHO | ||
| C. | 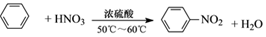 | D. | CH≡CH+HCl$→_{△}^{催化剂}$CH2=CHCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
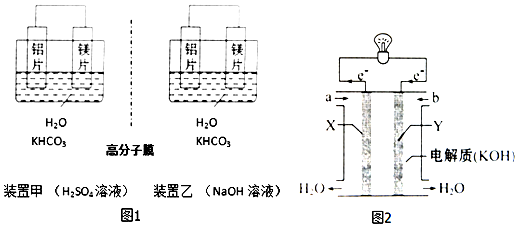
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 正戊烷、异戊烷、新戊烷的沸点依次降低 | |
| B. | 相对分子质量为104的烃,分子中不可能只存在单键 | |
| C. | 光照下2,2-二甲基丙烷与 Br2反应其二溴取代物有三种 | |
| D. | FeCl3溶液可以把 4 种无色溶液:乙醇、苯酚、AgNO3溶液、KOH 溶液一一区分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中,NO3-、Na+、I-、Fe2+ | |
| B. | 有CO32-存在的溶液中:Na+、Al3+、Ca2+、Br - | |
| C. | 有SCN-存在的溶液中:NH4+、Ba2+、Fe3+、Cl - | |
| D. | pH=13的无色透明溶液中,K+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 共价键 | C-H | H-H | C≡C |
| 键能/kJ•mol-1 | 431.4 | 436 | 812 |
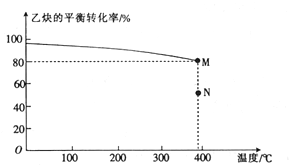
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com