
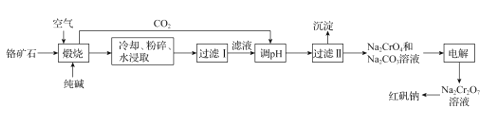
【题目】以铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)为原料制取红矾钠 (Na2Cr2O7·2H2O)的流程如图所示。
已知:I.Cr2O3在碱性条件下易被氧化;
II.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3 +Na2CO3=2NaAlO2 +CO2↑;
III.2CrO42-+2H+![]() Cr2O72- +H2O K=1.0×1012
Cr2O72- +H2O K=1.0×1012
(1)“煅烧”时,Cr2O3参加反应的化学方程式为_____。若“煅烧”操作最适宜的温度是800~900℃,则在实验室中进行此项操作时,应选择_____坩埚(填字母)。
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有_____(填化学式)。
(3)“过滤II”所得沉淀主要有______(填化学式)。
(4)由Na2Cr2O7溶液制备红矾钠的具体实验操作有_____,经洗涤、干燥得到红矾钠样品。
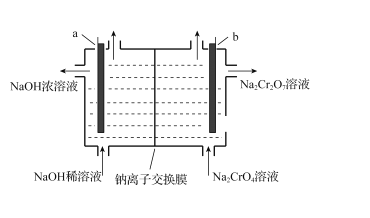
(5)“电解”时,利用以下装置将Na2CrO4溶液转化为Na2Cr2O7溶液,当a、b均为石墨电极时,a电极的电极反应式为____。若初始加入电解池中的c (Na2CrO4)=1.0mol·L-l,随着“电解”的进行,当溶液pH=6时,Na2CrO4的转化率为______(忽略电解过程中溶液体积变化)。
【答案】2Cr2O3+4Na2CO3+3O2![]() 4Na2CrO4+4CO2 d Na2CO3 H2SiO3、AI(OH)3 加热浓缩、冷却结晶、过滤 2H2O+2e-=2OH-+H2(或2H++2e-=H2) 50%
4Na2CrO4+4CO2 d Na2CO3 H2SiO3、AI(OH)3 加热浓缩、冷却结晶、过滤 2H2O+2e-=2OH-+H2(或2H++2e-=H2) 50%
【解析】
将铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)和纯碱、空气煅烧,发生反应得到NaAlO2、Na2CrO4、Na2SiO3、Na2CO3,然后水浸、过滤得到浸出液,浸出液中溶质是NaAlO2、Na2CrO4、Na2SiO3、Na2CO3 ,在浸出液中利用焙烧产生的二氧化碳调整溶液pH ,依据流程可知,溶液中偏铝酸钠、Na2SiO3生成硅酸沉淀和氢氧化铝沉淀,然后过滤得到滤液和沉淀,沉淀是H2SiO3、AI(OH)3,滤液中含有Na2CrO4和Na2CO3 ,加入酸继续调节溶液的pH ,根据信息②知,溶质变为Na2Cr2O7,将混合溶液蒸发浓缩、冷却结晶得到Na2Cr2O7晶体。
(1)根据流程和上述分析,“煅烧’’时,Cr2O3与加入的纯碱、空气高温下反应生成Na2CrO4和二氧化碳,化学反应方程式为:2Cr2O3+4Na2CO3+3O2![]() 4Na2CrO4+4CO2;陶瓷、玻璃、石英当中都含有二氧化硅,煅烧时加入的纯碱会与二氧化硅反应,损坏实验装置,因此因该在铁坩埚中进行煅烧操作。
4Na2CrO4+4CO2;陶瓷、玻璃、石英当中都含有二氧化硅,煅烧时加入的纯碱会与二氧化硅反应,损坏实验装置,因此因该在铁坩埚中进行煅烧操作。
答案为:2Cr2O3+4Na2CO3+3O2![]() 4Na2CrO4+4CO2 ;d
4Na2CrO4+4CO2 ;d
(2)流程图中。“过滤II”后得到溶液中含有Na2CO3,将混合溶液蒸发浓缩、冷却结晶得到Na2Cr2O7晶体后得到的滤液中含有大量Na2CO3可用于煅烧操作。
答案为:Na2CO3;
(3)浸出液中利用焙烧产生的二氧化碳调整溶液pH ,二氧化碳溶于水溶液显酸性,滤液中的偏铝酸钠、Na2SiO3转化为硅酸沉淀和氢氧化铝沉淀。
答案为:H2SiO3、AI(OH)3;
(4)由Na2Cr2O7溶液制备红矾钠固体,操作为蒸发浓缩、冷却结晶、过滤洗涤。
答案为:蒸发浓缩、冷却结晶、过滤;
(5)根据电解池中a电极端,加入稀氢氧化钠,相当于电解水,流出浓氢氧化钠,说明a电极周围产生大量氢氧根离子,因此可得a电极上水中氢离子得到电子转变为氢气和氢氧根,因此电极a为阴极,电极式为2H2O+2e-=2OH-+H2(或2H++2e-=H2);b电极为阳极,溶液中阴离子放电,根据放电顺序氢氧根大于含氧酸根(CrO42-),因此b电极为水中的氢氧根离子失去电子转变为氧气和氢离子,在氢离子存在的情况下,根据已知信息2CrO42-+2H+![]() Cr2O72- +H2O K=1.0×1012可得,
Cr2O72- +H2O K=1.0×1012可得,![]() ,溶液的pH=6,即
,溶液的pH=6,即![]() =1.0×10-6mol/L,K=
=1.0×10-6mol/L,K=![]() =
= =
= =1.0×1012,
=1.0×1012,![]() =0.5mol/L,因此当溶液pH=6时,溶液中剩余的CrO42-为0.5mol,消耗的CrO42-为0.5mol,Na2CrO4的转化率=
=0.5mol/L,因此当溶液pH=6时,溶液中剩余的CrO42-为0.5mol,消耗的CrO42-为0.5mol,Na2CrO4的转化率=![]() =50%;
=50%;
答案为:2H2O+2e-=2OH-+H2(或2H++2e-=H2);50%;


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】m、n、x、y四种主族元素在周期表的相对位置如图所示。已知它们的原子序数总和为46,则:
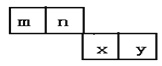
(1)元素n的气态氢化物的电子式为___,基态n原子的核外共有__种不同运动状态的电子。
(2)m与y所形成的化合物含___键,属___分子。(填“极性”或“非极性”)
(3)x位于周期表的第___周期第___族;其简单离子的离子结构示意图为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型可逆电池的工作原理如下图所示。放电时总反应为:Al+3Cn(AlCl4)+4AlCl4-![]() 4Al2Cl7-+3Cn(Cn表示石墨)。
4Al2Cl7-+3Cn(Cn表示石墨)。

下列说法正确的是
A. 放电时负极反应为:2Al-6e-+7Cl-= Al2Cl7-
B. 放电时AlCl4-移向正极
C. 充电时阳极反应为: AlCl4-e-+Cn=Cn(AlCl4)
D. 电路中每转移3mol电子,最多有1molCn(AlCl4)被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数,下列叙述正确的是( )
表示阿伏加德罗常数,下列叙述正确的是( )
A.3molFe在过量的纯氧中完全燃烧,转移的电子数为![]()
B.52g苯乙烯中含有的碳碳双键数目为![]()
C.标准状况下,![]() 和
和![]() 的混合气体的分子数目为
的混合气体的分子数目为![]()
D.![]() 溶液中
溶液中![]() 和
和![]() 的总数为
的总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害。某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示。下列判断正确的是
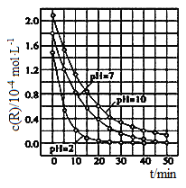
A. 在0~20min之间,pH=7时R的降解速率为0.07mol·L-1·min-1
B. R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响
C. 二氧化钛对pH=2的R溶液催化效率好
D. 在0~50 min之间,R的降解百分率pH=2大于pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,科学家合成了含有N![]() 的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )
的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示,以下有关该物质的说法中正确的是( )

A.每个N![]() 中含有35个质子和36个电子
中含有35个质子和36个电子
B.该离子中有非极性键和配位键
C.该离子中含有2个π键
D.与PCl![]() 互为等电子体
互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式为________________。
②NO![]() 的空间构型__________(用文字描述)。
的空间构型__________(用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①CO分子的等电子体有______。(至少写两个)
②HCHO分子中C原子轨道的杂化类型为______。
③1 mol CO2中含有的σ键与π键数目之比为_____。
④CO还能以配体形式与金属形成配合物,如Fe(CO)5,1mol Fe(CO)5中π键数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学工作者研发了一种 SUNCAT的系统,借助锂循环可持续合成氨,其原理如图所示。下列说法不正确的是

A.过程I得到的Li3N的电子式为 ![]()
B.过程Ⅱ生成W的反应为Li3N+3H2O=3LiOH+NH3↑
C.反应Ⅲ中能量转化的方式是电能转变为化学能
D.过程I、Ⅱ、Ⅲ均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个实验室制取氯气并以氯气为原料进行一系列反应的装置,回答下列问题。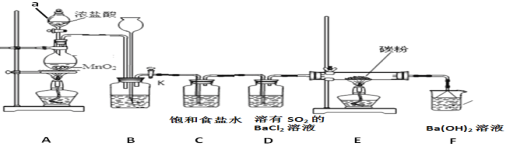
(1)写出a仪器的名称_______;
(2)装置D产生白色沉淀现象的原因_______________________;
(3)E装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,其产物为CO2和HCl。试写出E中反应的化学方程式_________________________________;
(4)F处的烧杯溶液中最终____(填“有”或“没有”)白色沉淀;
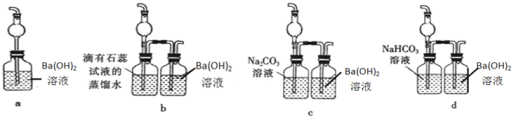
(5)F装置无法确认E处反应中有CO2产生,为了证明CO2的存在,要对F装置进行改造,装置符合要求的是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com