
”¾ĢāÄæ”湤ŅµÉĻĄūÓĆ“ÖZnO(ŗ¬FeO”¢CuO)ÖĘČ”½šŹōŠæµÄĮ÷³ĢČēĻĀ(²æ·Ö²½Ö菔ĀŌ):

ŅŃÖŖ£ŗ¼øÖÖĄė×ÓŠĪ³ÉĒāŃõ»ÆĪļ³ĮµķŹ±µÄpHČēĻĀ±ķ:
“ż³ĮµķµÄĄė×Ó | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
æŖŹ¼³ĮµķŹ±pH | 6.3 | 1.5 | 6.2 | 5.2 |
³ĮµķĶźČ«Ź±pH | 9.7 | 3.2 | 8.0 | 6.4 |
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ėį½ž“ÖŃõ»ÆŠæµÄ¹ż³ĢÖŠ£¬³£½«“ÖŃõ»ÆŠæ·ŪĖé³ÉĻøæÅĮ££¬ŹŹµ±Ōö¼ÓĮņĖįµÄÅØ¶Č£¬ÄæµÄŹĒ_________”£
£Ø2£©²½ÖčAµÄÄæµÄŹĒ½«Fe2+Ńõ»ÆĪŖFe3+,²¢Č«²æŠĪ³ÉFe(OH)3³Įµķ,ĪŖĮĖŌŻ²»ŠĪ³ÉCu(OH)2 Zn(OH)2 ,øĆ²½ÖčŠčæŲÖĘČÜŅŗpHµÄ·¶Ī§ŹĒ____________,øĆ²½ÖčÖŠĻČ¼ÓČėH2O2³ä·Ö·“Ó¦ŗóŌŁ¼ÓČė°±Ė®£¬Š“³ö¼ÓČėH2O2µÄĄė×Ó·½³ĢŹ½_____________”£
£Ø3£©²½ÖčCµÄ·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ____________”£
£Ø4£©Čō²½ÖčAÖŠ¼ÓČėH2O2ŗó£¬ŹŅĪĀĻĀ½«ČÜŅŗµÄpHµ÷ĪŖ4£¬ĒóFe3+ Ąė×ÓÅضČĪŖ_________”££ØŅŃÖŖKsp[Fe(OH)3]= 4.0”Į10-3 8£©
”¾“š°ø”æ¼Óæģ·“Ó¦ĖŁĀŹ 3. 2”ÜpH£¼5.2 2Fe2++H2O2+2H+=2Fe3++2H2O Cu2+ + Zn = Zn2+ + Cu 4 ”Į10-8
”¾½āĪö”æ
(1)øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ£¬Ėį½ž“ÖŃõ»ÆŠæµÄ¹ż³ĢÖŠ£¬ĪŖĮĖ¼ÓæģĖį½žĖŁĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ½«“ÖŃõ»ÆŠæ·ŪĖé³ÉĻøæÅĮ£”¢ŹŹµ±Ōö¼ÓĮņĖįµÄÅØ¶Č”¢ŹŹµ±ÉżøßĪĀ¶ČµČ£¬¹ŹÄæµÄŹĒ¼Óæģ·“Ó¦ĖŁĀŹ£»
(2)ĒāŃõ»ÆĢś³ĮµķŹ±µÄpHŹĒ1.48 ~ 3.2 £¬Zn(OH)2³ĮµķŹ±µÄpHĪŖ6.2 ~ 8.0£¬ŗĶCu(OH)2³ĮµķŹ±µÄpHĪŖ5.2~6.4£¬Ņņ“Ė½«Fe2+Ńõ»ÆĪŖFe3+£¬²¢Č«²æŠĪ³ÉFe(OH)3³Įµķ£¬ĪŖĮĖŌŻ²»ŠĪ³ÉCu(OH)2”¢Zn(OH)2 £¬øĆ²½ÖčŠčæŲÖĘČÜŅŗpHµÄ·¶Ī§ĪŖ3.2<pH<5.2£¬¼ÓČėH2O2 £¬·¢Éś¹żŃõ»ÆĒāŃõ»ÆŃĒĢśĄė×ӵķ“Ó¦£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Fe2++H2O2+2H+=2Fe3++2H2O£»
(3)²½ÖčCÖŠ¼ÓČėŠæ£¬·¢ÉśŠæŗĶĮņĖįĶ·“Ӧɜ³ÉĶŗĶĮņĖįŠæ£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖCu2++Zn=Zn2++Cu£»
(4) Čō²½ÖčAÖŠ¼ÓČėH2O2ŗó£¬ŹŅĪĀĻĀ½«ČÜŅŗµÄpHµ÷ĪŖ4£¬c£ØH+£©=10-4mol/L£¬c(OH-)=10-10mol/L£¬Ksp[Fe(OH)3]= c(Fe3+)c3(OH-)= c(Fe3+)”Į (10-10mol/L) 3=4.0”Į10-38£¬¹Źc(Fe3+)=4.0”Į10-8 mol/L”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø Äæ±ź²āŹŌĻµĮŠ“š°ø
Äæ±ź²āŹŌĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æäå±½ŹĒ²»ČÜÓŚĖ®µÄŅŗĢ壬³£ĪĀĻĀ²»ÓėĖį”¢¼ī·“Ó¦£¬æÉÓĆČēĶ¼×°ÖĆÖĘČ”£ØøĆ·“Ó¦·Å³öČČĮ棩”£ÖĘČ”Ź±¹Ū²ģµ½ÉÕĘæÖŠÓŠ“óĮæŗģ×ŲÉ«ÕōĘų£¬×¶ŠĪĘæÖŠµ¼¹ÜæŚÓŠ°×Īķ³öĻÖµČĻÖĻó”£
![]()

ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A£®Öʱøäå±½µÄ·“Ó¦ŹōÓŚČ”“ś·“Ó¦
B£®°×Īķ³öĻÖŹĒŅņĪŖHBrŅ×»Ó·¢ĒŅ¼«Ņ×ČÜÓŚĖ®
C£®×°ÖĆĶ¼ÖŠ³¤Ö±²£Į§µ¼¹Ü½öĘšµ¼Ęų×÷ÓĆ
D£®äå±½ÖŠČÜÓŠÉŁĮæµÄä壬æÉÓĆNaOHČÜŅŗĻ“µÓ³żČ„
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖŃŠ¾æĢ¼ĖįøĘÓėŃĪĖį·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ä³Ķ¬Ń§ĶعżŹµŃé²ā¶ØĢ¼ĖįøĘ¹ĢĢåÓė×ćĮæĻ”ŃĪĖį·“Ӧɜ³ÉCO2µÄĢå»żĖꏱ¼äµÄ±ä»ÆĒéæö£¬»ęÖĘ³öĻĀĶ¼ĖłŹ¾µÄĒśĻß”£ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ²»ÕżČ·µÄŹĒ

A. ŌŚ0-t1”¢t1-t2”¢t2-t3ÖŠ£¬t1-t2Éś³ÉµÄCO2ĘųĢå×ī¶ą
B. Ņņ·“Ó¦·ÅČČ£¬µ¼ÖĀ0-t1ÄŚµÄ·“Ó¦ĖŁĀŹÖš½„Ōö“ó
C. t2-t3µÄĖŁĀŹV(CO2)= ![]() mL/s
mL/s
D. ½«Ģ¼ĖįøĘ¹ĢĢåŃŠ³É·ŪÄ©£¬ŌņĒśĻß¼×½«±ä³ÉĒśĻßŅŅ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ![]() ŹĒ¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹µÄ¶ĢÖÜĘŚŌŖĖŲŠĪ³ÉµÄ¼ņµ„Ąė×Ó”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
ŹĒ¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹µÄ¶ĢÖÜĘŚŌŖĖŲŠĪ³ÉµÄ¼ņµ„Ąė×Ó”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A.Ō×Ó°ė¾¶: C>D>A>BB.Ō×ÓŠņŹż: b>a>d>c
C.Ąė×Ó°ė¾¶: D>C>A>BD.µ„ÖŹ»¹ŌŠŌ: A>B>C>D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śæĘѧ¼ŅŃŠ·¢ĮĖŅ»ÖÖŹŅĪĀĻĀ”°æÉŗōĪü”±µÄNa”ŖCO2¶ž“Īµē³Ų”£½«NaClO4ČÜÓŚÓŠ»śČܼĮ×÷ĪŖµē½āŅŗ£¬ÄĘŗĶøŗŌŲĢ¼ÄÉĆ׹ܵÄÄųĶų·Ö±š×÷ĪŖµē¼«²ÄĮĻ£¬µē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ3CO2+4Na![]() 2Na2CO3+C”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
2Na2CO3+C”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A. ·ÅµēŹ±£¬ClO4£Ļņøŗ¼«ŅʶÆ
B. ³äµēŹ±ŹĶ·ÅCO2£¬·ÅµēŹ±ĪüŹÕCO2
C. ·ÅµēŹ±£¬Õż¼«·“Ó¦ĪŖ£ŗ3CO2+4e £½2CO32£+C
D. ³äµēŹ±£¬Õż¼«·“Ó¦ĪŖ£ŗNa++e£½Na
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·“Ó¦4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)ŌŚ5LĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗó£¬NOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬Ōņ“Ė·“Ó¦µÄĘ½¾łĖŁĀŹ
4NO(g) + 6H2O(g)ŌŚ5LĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗó£¬NOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬Ōņ“Ė·“Ó¦µÄĘ½¾łĖŁĀŹ![]() x
x
A. ![]() (O2) = 0.01mol”¤(L”¤s) ØC1 B.
(O2) = 0.01mol”¤(L”¤s) ØC1 B. ![]() (NO) = 0.008mol”¤(L”¤s) ØC1
(NO) = 0.008mol”¤(L”¤s) ØC1
C. ![]() (H2O) = 0.006mol”¤(L”¤s) ØC1 D.
(H2O) = 0.006mol”¤(L”¤s) ØC1 D. ![]() (NH3) = 0.002mol”¤(L”¤s) ØC1
(NH3) = 0.002mol”¤(L”¤s) ØC1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æK3[Fe(C2O4)3]”¤3H2O£ØČż²ŻĖįŗĻĢśĖį¼Ų£©ĪŖĮĮĀĢÉ«¾§Ģ壬æÉÓĆÓŚÉ¹ÖĘĄ¶Ķ¼”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©É¹ÖĘĄ¶Ķ¼Ź±£¬ÓĆK3[Fe(C2O4)3]”¤3H2O×÷øŠ¹ā¼Į£¬ŅŌK3[Fe(CN)6]ČÜŅŗĪŖĻŌÉ«¼Į”£Ęä¹ā½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2K3[Fe(C2O4)3]![]() 2FeC2O4+3K2C2O4+2CO2”ü£»ĻŌÉ«·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______________”£
2FeC2O4+3K2C2O4+2CO2”ü£»ĻŌÉ«·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______________”£
£Ø2£©Ä³Š”×éĪŖĢ½¾æČż²ŻĖįŗĻĢśĖį¼ŲµÄČČ·Ö½ā²śĪļ£¬°“ĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ锣

¢ŁĶØČėµŖĘųµÄÄæµÄŹĒ________________________________________”£
¢ŚŹµŃéÖŠ¹Ū²ģµ½×°ÖĆB”¢FÖŠ³ĪĒåŹÆ»ŅĖ®¾ł±ä»ė×Ē£¬×°ÖĆEÖŠ¹ĢĢå±äĪŖŗģÉ«£¬ÓÉ“ĖÅŠ¶ĻČČ·Ö½ā²śĪļÖŠŅ»¶Øŗ¬ÓŠ___________”¢___________”£
¢ŪĪŖ·ĄÖ¹µ¹Īü£¬Ķ£Ö¹ŹµŃ鏱Ӧ½ųŠŠµÄ²Ł×÷ŹĒ_____________________________”£
¢ÜѳʷĶźČ«·Ö½āŗó£¬×°ÖĆAÖŠµÄ²ŠĮōĪļŗ¬ÓŠFeOŗĶFe2O3£¬¼ģŃéFe2O3“ęŌŚµÄ·½·ØŹĒ£ŗ________________”£
£Ø3£©²ā¶ØČż²ŻĖįŗĻĢśĖį¼ŲÖŠĢśµÄŗ¬Į攣
¢Ł³ĘĮæm gѳʷӌ׶ŠĪĘæÖŠ£¬Čܽāŗó¼ÓĻ”H2SO4Ėį»Æ£¬ÓĆc mol”¤L-1 KMnO4ČÜŅŗµĪ¶ØÖĮÖÕµć”£µĪ¶ØÖÕµćµÄĻÖĻóŹĒ___________________________”£
¢ŚĻņÉĻŹöČÜŅŗÖŠ¼ÓČė¹żĮæŠæ·ŪÖĮ·“Ó¦ĶźČ«ŗ󣬹żĀĖ”¢Ļ“µÓ£¬½«ĀĖŅŗ¼°Ļ“µÓŅŗČ«²æŹÕ¼Æµ½×¶ŠĪĘæÖŠ”£¼ÓĻ”H2SO4Ėį»Æ£¬ÓĆc mol”¤L-1 KMnO4ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄKMnO4ČÜŅŗV mL”£øĆ¾§ĢåÖŠĢśµÄÖŹĮæ·ÖŹżµÄ±ķ“ļŹ½ĪŖ________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬ĻņAŗĶBÖŠ¶¼³äČĖ2molXŗĶ2molY£¬ĘšŹ¼VA=0.8a L£¬VB=a L±£³ÖĪĀ¶Č²»±ä£¬ŌŚÓŠ“߻ƼĮµÄĢõ¼žĻĀ£¬Į½ČŻĘ÷ÖŠø÷×Ō·¢ÉśĻĀĮŠ·“Ó¦£ŗX(g)+Y(g)![]() 2Z(g)+W(g)“ļµ½Ę½ŗāŹ±£¬VA=0.9a L£¬ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ ( )
2Z(g)+W(g)“ļµ½Ę½ŗāŹ±£¬VA=0.9a L£¬ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ ( )
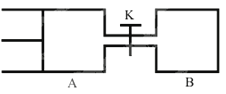
A. Į½ČŻĘ÷ÖŠ“ļµ½Ę½ŗāµÄŹ±¼äA<B
B. “ņæŖK“ļµ½ŠĀĘ½ŗāŗó£¬ÉżøßBČŻĘ÷ĪĀ¶Č,AČŻĘ÷Ģå»żĻą±ČŌĘ½ŗāדĢ¬Ź±Ņ»¶ØŌö“ó
C. AČŻĘ÷ÖŠXµÄ×Ŗ»ÆĀŹĪŖ25%£¬ĒŅ±ČBČŻĘ÷ÖŠµÄXµÄ×Ŗ»ÆĀŹŠ”
D. “ņæŖKŅ»¶ĪŹ±¼ä“ļĘ½ŗāŹ±£¬AµÄĢå»żĪŖ0.8a L£ØĮ¬ĶعÜÖŠµÄĘųĢåĢå»ż²»¼Ę£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņĮ½·Ż30mLĶ¬Ņ»ÅØ¶ČµÄNaOHČÜŅŗÖŠĶØČėCO2ĘųĢ壬ŅņCO2ĶØČėĮæµÄ²»Ķ¬£¬ČÜŅŗµÄ×é³ÉŅ²²»Ķ¬£¬µĆµ½ČÜŅŗM”¢N”£ČōĻņM”¢NČÜŅŗÖŠÖšµĪ¼ÓČėÅضČĪŖ0.25mol”¤L£1ŃĪĖį£¬²śÉśµÄĘųĢåĢå»żv(CO2)Óė¼ÓČėŃĪĖįµÄĢå»żv(HCl)µÄ¹ŲĻµ·Ö±šĪŖČēĶ¼ĖłŹ¾Į½ÖÖĒéæöAŗĶB”£
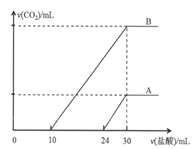
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©MČÜŅŗÖŠČÜÖŹĪŖ(Š“»ÆѧŹ½)___________£¬ĘäĪļÖŹµÄĮæÖ®±ČŹĒ__________”£
£Ø2£©NČÜŅŗČÜÖŹĪŖ(Š“»ÆѧŹ½)____________£¬±ź×¼×“æöĻĀCO2ĘųĢåµÄĢå»żĪŖ________£¬ŌNaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ_________ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com