
| A£® | CaO2¾ßÓŠŃõ»ÆŠŌ£¬¶ŌĆę·ŪæÉÄܾßÓŠŌö°××÷ÓĆ | |
| B£® | CaO2ÓėĖ®·“Ó¦Ź±£¬Ćæ²śÉś1molO2×ŖŅʵē×Ó4mol | |
| C£® | CaO2ÖŠŅõŃōĄė×ÓµÄøöŹż±ČĪŖ1£ŗ1 | |
| D£® | CaO2ÓėCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2CaO2+2CO2ØT2CaCO3+O2 |
·ÖĪö A”¢ŅĄ¾Ż¹żŃõ»ÆÄʵĊŌÖŹĶʶĻ¹żŃõ»ÆøʵĊŌÖŹæÉÄܾßÓŠĘư׊Ō£»
B”¢ŅĄ¾ŻCaO2ŗĶĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½·ÖĪö¼ĘĖć£»
C”¢ŅĄ¾Ż¹żŃõ»ÆøĘ¹¹³ÉĄė×ÓŹĒÄĘĄė×ÓŗĶ¹żŃõøłĄė×Ó·ÖĪö£»
D”¢ŅĄ¾Ż¹żŃõ»ÆÄĘŠŌÖŹĶʶĻ¹żŃõ»ÆøĘÓė¶žŃõ»ÆĢ¼µÄ·“Ó¦£®
½ā“š ½ā£ŗA”¢½įŗĻ¹żŃõ»ÆÄʵĊŌÖŹĶʶĻ£¬CaO2¾ßÓŠŃõ»ÆŠŌ£¬æÉÄܾßÓŠĘư׊Ō£¬¶ŌĆę·ŪæÉÄܾßÓŠŌö°××÷ÓĆ£¬¹ŹAÕżČ·£»
B”¢CaO2ŗĶĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2CaO2+2H2O=2Ca£ØOH£©2+O2”ü£¬Ćæ²śÉś1molO2×ŖŅʵē×Ó2mol£¬¹ŹB“ķĪó£»
C”¢¹żŃõ»ÆøĘ¹¹³ÉĄė×ÓŹĒÄĘĄė×ÓŗĶ¹żŃõøłĄė×Ó£¬CaO2ÖŠŅõŃōĄė×ÓµÄøöŹż±ČĪŖ1£ŗ1£¬¹ŹCÕżČ·£»
D”¢CaO2ŗĶCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2CaO2+2CO2=2CaCO3+O2£¬¹ŹDÕżČ·£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ¹żŃõ»ÆĪļŠŌÖŹµÄĶʶĻÓ¦ÓĆ£¬ŅĄ¾Ż¹żŃõ»ÆÄʵĊŌÖŹ·ÖĪöĄąĶĘ¹żŃõ»ÆøʵĊŌÖŹŹĒ½āĢā¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
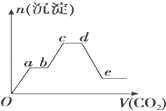 ½«×ćĮæµÄCO2²»¶ĻĶØČėKOH”¢Ba£ØOH£©2”¢KAlO2µÄ»ģŗĻČÜŅŗÖŠ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓėĖłĶØČėCO2µÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠ¹ŲÓŚÕūøö·“Ó¦¹ż³ĢÖŠµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©
½«×ćĮæµÄCO2²»¶ĻĶØČėKOH”¢Ba£ØOH£©2”¢KAlO2µÄ»ģŗĻČÜŅŗÖŠ£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓėĖłĶØČėCO2µÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠ¹ŲÓŚÕūøö·“Ó¦¹ż³ĢÖŠµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Oa¶Ī·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒBa£ØOH£©2+CO2ØTBaCO3”ż+H2O | |
| B£® | ab¶ĪÓėcd¶Ī³ĮµķÖŹĮ涼²»±ä£¬µ«Ėł·¢ÉśµÄ·“Ó¦²»ĻąĶ¬ | |
| C£® | bc¶Ī·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ2AlO2-+3H2O+CO2ØT2Al£ØOH£©3”ż+CO32- | |
| D£® | de¶Ī³Įµķ¼õÉŁŹĒÓÉÓŚAl£ØOH£©3¹ĢĢåĻūŹ§µÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū | B£® | ¢Ł¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 L°±ĘųĢå·Ö½ā³É1 LµŖĘųÓė3 LĒāĘųĪüŹÕ92 kJČČĮæ | |
| B£® | 1 molµŖĘųÓė3 molĒāĘų·“Ӧɜ³É2 molŅŗĢ¬°±·Å³öµÄČČĮæŠ”ÓŚ92 kJ | |
| C£® | 25”ęŗĶ101kPaŹ±£¬2 molNH3£Øg£©ĶźČ«·Ö½āĪŖ1 mol N2£Øg£©ŗĶ3 mol H2£Øg £©ĪüČČ92KJ | |
| D£® | 3øöĒāĘų·Ö×ÓÓė1øöµŖĘų·Ö×Ó·“Ӧɜ³É2øö°±Ęų·Ö×ӷųö92 kJČČĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8.4 | B£® | 9.6 | C£® | 6 | D£® | 9.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā



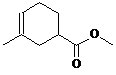 Ӣ
”¢ £®
£®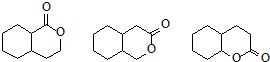 ČĪŅāŅ»ÖÖ£®
ČĪŅāŅ»ÖÖ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®ÕōĘųĶعż×ĘČȵÄĢś·Ū | B£® | ¶žŃõ»ÆĢ¼ĶعżNa2O2·ŪÄ© | ||
| C£® | ½«Znʬ·ÅČėCuSO4ČÜŅŗ | D£® | ĀĮÓėMnO2·¢ÉśĀĮČČ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
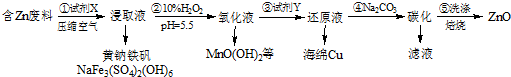
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com