
【题目】最近热播剧《外科风云》中利多卡因药物引发的医疗问题扑朔迷离,盐酸利多卡因(F)葡萄糖注射液,可用于抗心律失常。其合成路线如下:

(1)写出A的名称______________________。
(2)B在核磁共振氢谱上有_______种特征峰。
(3)C的结构简式为______________________;C→D的反应类型是________________。
(4)B有多种同分异构体,符合以下条件的B的同分异构体(不包括B本身)共有_______________种,请写出其中一种的结构简式_____________________。
①苯环上共有三个取代基 ②与碳酸钠溶液反应可放出CO2气体
(5)1mol D与足量的NaOH溶液共热反应,最多消耗NaOH的物质的量为_____mol。
(6)对氨基苯甲酸是机体细胞生长和分裂所必需的叶酸的组成成分。现以甲苯为原料,结合题干有关信息,补充完成以下合成路线:_______

【答案】 间二甲苯或1,3-二甲苯 3 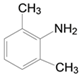 取代反应 10种
取代反应 10种 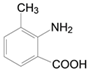 10种中的任意一种均给分 2
10种中的任意一种均给分 2 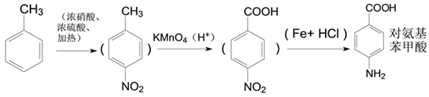 第一步也可以按题中信息写
第一步也可以按题中信息写
【解析】由B可知A应为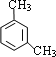 ,A与浓硝酸在浓硫酸的作用下发生硝化反应生成B,B发生还原反应生成C,结合D的结构简式可知,C取代反应生成D,则C为
,A与浓硝酸在浓硫酸的作用下发生硝化反应生成B,B发生还原反应生成C,结合D的结构简式可知,C取代反应生成D,则C为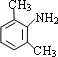 ,由E的结构简式可知,D中氯原子为-N(C2H5)2取代生成E,E转化得到F,则
,由E的结构简式可知,D中氯原子为-N(C2H5)2取代生成E,E转化得到F,则
(1)根据以上分析可知A是间二甲苯或1,3-二甲苯;(2)B结构对称,含有3种不同的H原子,其核磁共振氢谱中含有3种特征峰;(3)根据以上分析可知C的结构简式为 ;对比C、D的结构简式,是-NH2→
;对比C、D的结构简式,是-NH2→![]() ,应为取代反应;(4)B为
,应为取代反应;(4)B为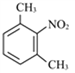 ,对应的同分异构体满足:①苯环上共有三个取代基;②与碳酸钠溶液反应可放出CO2气体,说明分子中含有-COOH,另外还含有取代基为-NH2、-CH3,依据定二议一可知有10种不同的结构,例如
,对应的同分异构体满足:①苯环上共有三个取代基;②与碳酸钠溶液反应可放出CO2气体,说明分子中含有-COOH,另外还含有取代基为-NH2、-CH3,依据定二议一可知有10种不同的结构,例如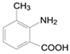 ;(5)D中含有肽键和氯原子,因此1mol D与足量的NaOH溶液共热反应,最多消耗NaOH的物质的量为2mol。(6)要引入氨基需要首先引入硝基,即甲苯首先发生硝化反应生成对甲基硝基苯,然后利用酸性高锰酸钾溶液氧化甲基转化为羧基,最后利用铁和盐酸将硝基还原为氨基,合成路线为
;(5)D中含有肽键和氯原子,因此1mol D与足量的NaOH溶液共热反应,最多消耗NaOH的物质的量为2mol。(6)要引入氨基需要首先引入硝基,即甲苯首先发生硝化反应生成对甲基硝基苯,然后利用酸性高锰酸钾溶液氧化甲基转化为羧基,最后利用铁和盐酸将硝基还原为氨基,合成路线为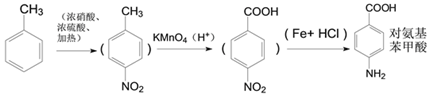 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】位于短周期的四种元素A、B、C、D,它们的原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。回答下列问题:
(1)上述元素可以形成多种具有漂白性的物质,请写出任意两种物质的化学式:_________,______________;
(2)C与D形成D的最低价化合物的电子式:_________ ;
(3)写出C与水反应的离子方程式:______________________________;
(4)A、B组成的物质E可形成甲、乙两种微粒,它们均有10个电子。写出E生成甲、乙的方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Fe , Cu的混合物中加入一定量的稀硝酸并微热,充分反应后剩余金属a克。再向其中加入一定量的稀盐酸并加热,充分振荡后还剩余金属b克。则[
A.a一定大于bB.a一定等于b C.a可能小于bD.a可能等于b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.葡萄糖和麦芽糖属于还原性糖
B.用新制的银氨溶液可区分甲酸和乙醛
C.乙烯和苯都能使溴水褪色,褪色的原因相同
D.淀粉和纤维素的化学式均为(C6H10O5)n,两者都能在人体内水解生成葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pOH值指的是溶液的碱度,以溶液中OH-浓度来表示,与pH所表示的溶液酸度相对应,pOH等于OH-的浓度的负常用对数。下图分别表示的是在25℃和100℃下水的电离平衡曲线。下列说法中正确的是

A. 曲线B表示的是25°C时水的电离平衡曲线
B. 25°C时,向pH=1的稀硫酸中逐滴滴入pH=11的稀氨水至过量,反应过程中水的电离先促进后抑制
C. Q点对应的溶液中,可同时大量存在K+、Fe3+、NO3-、SO42-
D. 100°C时,将pH = 2的硫酸与pH=12的氧氧化钠溶液等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A. a g C2H4和C3H6的混合物所含原子总数为![]()
B. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
C. 标准状况下,22.4 L H2O含有的分子数为 NA
D. 物质的量浓度为0.5 mol·L1的MgCl2溶液中,含有Cl个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X和Y是同周期主族元素,X元素在第IA族,Y元素在第VA族,则X和Y两元素原子序数之差不可能是
A. 4 B. 14 C. 24 D. 28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、L、M为核电荷数依次增大的前20号主族元素。X2是最轻的气体,Y、L与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与L组成的最简单化合物的电子式为____________。
(2)X与M组成的物质为_____________(填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为__________。
(3)Y在周期表中的位置是____________,其含氧酸的化学式为______________。
(4)L与M形成的化合物中L的化合价是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空:
(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑥INaOH固体⑨SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩液氯 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。
(2)NaHSO4是一种酸式盐,请填写下列空白:
①NaHSO4晶体熔化时的电离方程式为______________________________。
②与0.1 mol·L-1的NaHSO4溶液的导电能力相同的硫酸溶液的物质的量浓度为:_______________。
③NaHSO4溶液与NaHCO3溶液反应的离子方程式为______________________________。
④3 mol·L-1 NaHSO4与2 mol·L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程式为________________________________________。
(3)等质量SO2和SO3的分子数之比为_____,同温同压下的密度之比为_____,含氧原子数之比为____。
(4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com