
【题目】下列括号中的分离方法运用不得当的是( )
A. 碳酸钠和碳酸钙(过滤)
B. 水溶液中的食盐和碘(分液)
C. 碳酸钙和氯化钙(溶解 过滤 蒸发)
D. 自来水中的杂质(蒸馏)
科目:高中化学 来源: 题型:
【题目】如图为相互串联的甲乙两电解池. 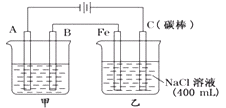
(1)甲池若为用电解原理精炼铜的装置,①A是极,材料是 , 电极反应为 , ②B是极,材料是 , 主要电极反应为 , 电解质溶液为 .
(2)写出乙池中发生的总反应的离子方程式 .
(3)若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为L.
(4)若此时乙池剩余液体为400mL,则电解后得到碱液的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3bMn(OH)2cH2O].
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 , 反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 .
(2)为测定碱式碳酸锰组成,取7.390g样品溶于硫酸,生成CO2224.0mL(标准状况),并配成500mL溶液.准确量取10.00mL该溶液,用0.0500molL﹣1EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2++H2Y2﹣=MnY2﹣+2H+),至终点时消耗EDTA标准溶液28.00mL.通过计算确定该样品的化学式.(写出计算过程) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,会产生明显的药品变质问题的是
A. NaNO3 B. FeCl2 C. Na2SO4 D. AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物X转化为Y和Z的能量变化如图所示.下列说法正确的是( ) 
A.由X→Y反应的△H=E5﹣E2
B.由X→Z反应的△H<0
C.降低压强有利于提高Y的产率
D.升高温度有利于提高Z的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+电子层结构与氖相同,Z的质子数为偶数,室温下M单质为淡黄色固体,回答下列问题:
(1)M元素位于周期表中的第周期、族.
(2)Z元素是 , 其在自然界中常见的二元化合物是 .
(3)X与M的单质在高温下反应的化学方程式为 , 产物分子为直线形,其化学键属共价键(填“极性”或“非极性”).
(4)四种元素中的可用于航空航天合金材料的制备,其单质与稀盐酸反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①碘的饱和水溶液 ②汽油和氯化钠溶液 ③碳酸钙和水。分离以上各混合液的正确方法依次是
A. 萃取、分液、过滤 B. 萃取、分液、蒸馏
C. 分液、蒸馏、过滤 D. 蒸馏、萃取、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究影响过氧化氢分解的因素,做了三个实验。相应的实验结果如下图所示,请分析回答:
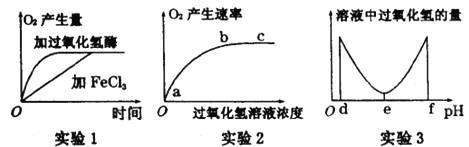
(1)实验1、2、3中的自变量分别为 。
(2)实验1的目的是探究 。
(3)实验2探究了过氧化氢溶液的浓度对过氧化氢酶的影响,该实验的结果显示 ,be段O2产生速率不再增大的原因最可能是 。
(4)实验3的结果显示,过氧化氢酶的最适pH为 。实验还证实,当pH小于d或大于f时,过氧化氢酶的活性将永久丧失,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示构成细胞的元素及其有不同有机化合物,a、b、c、d代表不同的小分子物质,A、B、C代表不同的大分子物质,请分析并回答下列问题:

(1)若A为植物细胞特有的储能物质,则A为__,在动物细胞内,与物质A作用最相近的是__。
(2)若物质A 在动植物细胞中均可含有,并且作为细胞内最理想的储能物质,则A是__。物质b的分子结构式__,鉴定物质B的试剂使用方法是__。
(3)物质c在动物细胞中共有__种,分子中__的不同决定了c的种类不同.物质d是__,它属于固醇类物质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com