
| A. | Cl-→Cl2 | B. | H2→H+ | C. | CuO→Cu | D. | Zn→Zn2+ |
分析 变化中需要加入还原剂才能实现,说明给予物质作氧化剂,在反应中得电子化合价降低,据此分析解答.
解答 解:A.该反应中Cl元素化合价由-1价变为0价,所以氯离子是还原剂,需要氧化剂才能实现,如高锰酸钾、二氧化锰等,故A错误;
B.该反应中H元素化合价由0价变为+1价,所以氢气是还原剂,需要氧化剂才能实现,如氧气等,故B错误;
C.该反应中Cu元素化合价由+2价变为0价,所以CuO是氧化剂,需要还原剂才能实现,如C、CO等,故C正确;
D.该反应中Zn元素化合价由0价变为+2价,所以锌是还原剂,需要氧化剂才能实现,如硫酸等,故D错误;
故选C.
点评 本题考查氧化还原反应,侧重考查基本概念,明确氧化剂、还原剂概念内涵及其与化合价变化关系是解本题关键,熟悉常见元素化合价,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 27mg | B. | 54mg | C. | 108mg | D. | 216mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol| A. | CO的燃烧热为283 kJ | |
| B. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g)△H=+452 kJ/mol | |
| C. | 如图可表示由CO生成CO2的反应过程和能量关系 | |
| D. | CO(g)与Na2O2(s)反应生成1molNa2CO3(s)时放出509kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氨水中滴入盐酸:H++OH-=H2O | |
| B. | 向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O | |
| C. | 稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
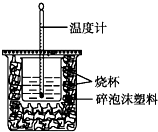 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c(Clˉ)为 4.00mol•L-1,c(Al3+)为1.00 mol•L-1 | |
| D. | c(Mg2+)为 1.00mol•L-1,c(Na+)为 0.50 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com