
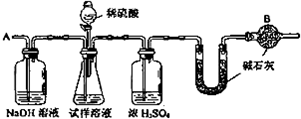
分析 (1)根据盐酸的挥发性考虑;
(2)就是为了将二氧化碳全部赶过去;
(3)根据U型管的质量的增加量就是生成的二氧化碳的质量,根据二氧化碳的质量算出碳酸钠的质量,再用碳酸钠的质量除以样品质量即可.
(4)可以根据用一种试剂与碳酸钠反应产生沉淀,根据沉淀算出碳酸钠的质量,再进行推算.
解答 解:(1)由于盐酸具有挥发性,也会随着二氧化碳进入U型管,被误认为是二氧化碳,所以二氧化碳的质量偏大,算出的碳酸钠的质量也会偏大的,所以结果会偏高,
故答案为:偏高;
(2)直到U型管的质量基本不变,说明二氧化碳已经被全部排到U型管中,步骤⑦的目的是:判断反应中的CO2是否全部排出,并被U型管中的碱石灰吸收,
故答案为:判断反应中的CO2是否全部排出,并被U型管中的碱石灰吸收;
(3)设需要碳酸钠的质量为X则:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
X d-b
列比例式:$\frac{106}{x}$=$\frac{44}{d-b}$
解得X=$\frac{106(d-b)}{44}$g
所以试样中纯碱的质量分数的计算式为$\frac{\frac{106(d-b)}{44}g}{ag}$×100%=$\frac{106(d-b)}{44a}$×100%,
故答案为:$\frac{106(d-b)}{44a}$×100%;
(4)根据用一种试剂与碳酸钠反应产生沉淀,根据沉淀算出碳酸钠的质量:取一定量试样放入烧杯中,加适量蒸馏水溶解,再向烧杯中滴加足量氯化钡溶液,将得到的沉淀过滤、洗涤、干燥后称量,根据方程式由沉淀质量算出碳酸钠质量,再除以样品质量.故答案为:取一定量的纯碱试样,溶入适量的蒸馏水中,加入足量的BaCl2溶液,过滤、洗涤、干燥、称量滤渣(BaCO3).
点评 本题考查物质组成的实验探究、含量测定与计算、过程分析判断,容易出错的地方是不设计干燥管B,忘记空气中的二氧化碳和水分也能够进入U型管中,会使结果偏大,题目难度中等.


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 锗是一种金属性很强的元素 | B. | 锗的单质具有半导体的性能 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗酸(H4GeO4)是难溶于水的弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol•L-1 H2SO4 | B. | pH=2的H2SO4溶液 | ||
| C. | c(OH-)=10-13mol•L-1 | D. | pH=1溶液加水稀释1倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | DMC的结构简式为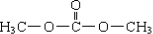 | |
| B. | DMC在空气不能燃烧 | |
| C. | DMC易溶于水,不溶于乙醇和丙酮 | |
| D. | DMC用于生产非毒性化工产品,故被誉为有机合成的“绿色化工原料” |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com