
【题目】补铁剂常用于防治缺铁性贫血,其有效成分一般为硫酸亚铁、琥珀酸亚铁、富马酸亚铁和乳酸亚铁等。回答下列问题:
(1)能表示能量最低的亚铁离子的电子排布式是_________(填标号)。
a.[Ar]3d54s2 b.[Ar]3d54s1 c.[Ar]3d64s2 d.[Ar]3d6
(2)琥珀酸即丁二酸(HOOCCH2CH2COOH),在琥珀酸分子中电负性最大的原子是_____,碳原子的杂化方式是______;琥珀酸亚铁中存在配位键,在该配位键中配位原子是____,中心原子是____。
(3)富马酸和马来酸互为顺反异构体,其电离常数如下表:
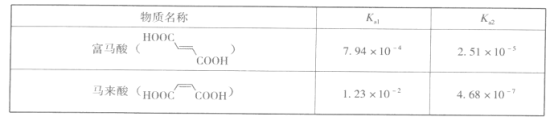
请从氢键的角度解释富马酸两级电离常数差别较小,而马来酸两级电离常数差别较大的原因:____。
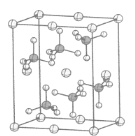
(4)β-硫酸亚铁的晶胞结构如图所示,其晶胞参数为a= 870 pm、b=680 pm、c=479 pm,α=β=γ=90°,Fe2+占据晶胞顶点、棱心、面心和体心。在该晶胞中,硫酸根离子在空间上有____种空间取向,晶胞体内硫酸根离子的个数是____,铁原子周围最近的氧原子的个数为____;设阿伏加德罗常数的值为NA,则该晶体的密度是____ g·cm-3(列出计算表达式)。
【答案】d O sp2、sp3 O Fe 马来酸中存在分子内氢键,提高了羧基的离子性,有利于酸性电离,因此马来酸电离主要以第一步电离为主 2 2 6 ![]()
【解析】
(1)绝大多数过渡元素中,同一元素的价态变化是连续的,因为(n-1)d和ns轨道的能量相差不大,可以逐个失去s电子和d电子造成氧化态的连续变化。基态铁原子核外电子排布式为[Ar]3d64s2,失去4s2变成亚铁离子,由此可得正确答案;
(2)同一周期,随着原子序数的增加,元素的电负性逐渐增大。C、O为同周期元素,H的电负性最小,由此可判断C、H、O的电负性的大小。根据中心原子的孤对电子数以及与中心原子相连的原子个数来判断分子中原子的杂化方式,可分析出丁二酸中C原子的杂化方式。琥珀酸亚铁中O原子有孤电子对,亚铁离子中存在空轨道,根据配合物中中心原子提供空轨道,配位原子必须是含有孤对电子的原子,可以判断出琥珀酸亚铁中配位原子和中心原子。
(3)在马来酸分子中,O原子吸引电子的能力较强,H-O共用电子对偏向O原子,从而提高了羧基的离子性,据此分析。
(4)利用“均摊法”计算晶胞拥有的粒子数目,根据公式xM=ρa3NA求算晶胞的密度。
(1)基态铁原子核外电子排布式为[Ar]3d64s2,失去2个电子后变为亚铁离子,基态亚铁离子核外电子排布式为[Ar]3d6,故能表示能量最低的亚铁离子的电子排布式为d。答案为:d;
(2)H、C、O中H元素的电负性最小,C、O为同周期元素,原子序数越大,电负性越大,因此电负性最大的是O;C原子连接4个原子形成共价键时,C原子采用sp3杂化,C原子连接3个原子形成共价键时,C原子采用sp2杂化。因此丁二酸中C原子的杂化方式为sp2、sp3杂化。丁二酸中只有O原子有孤电子对,亚铁离子中存在空轨道,故琥珀酸亚铁的配位键中配位原子为O原子,中心原子为Fe原子。答案为:O;sp2、sp3;O;Fe;
(3)马来酸存在分子内氢键,提高了羧基的离子性,有利于酸性电离,因此一级电离较为容易,而剩余部分因为形成了分子内氢键而很稳定,相对难易电离,因此马来酸电离主要以第一步电离为主。答案为:马来酸中存在分子内氢键,提高了羧基的离子性,有利于酸性电离,因此马来酸电离主要以第一步电离为主;
(4)分析晶胞结构,可知硫酸根离子在空间上的取向有2种: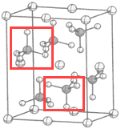 ,β-硫酸亚铁的化学式为FeSO4,晶胞中含有亚铁离子数目为
,β-硫酸亚铁的化学式为FeSO4,晶胞中含有亚铁离子数目为![]() ,则晶胞中所含硫酸根离子数目也为4,从晶胞示意图中可以发现有6个硫酸根离子,其中4个位于面上。故晶胞体内有2个硫酸根离子;以体心的亚铁离子为研究对象,每个硫酸根中均有一个氧原子离铁原子最近,亚铁离子周围最近的氧原子的个数为6;该晶胞的密度为:
,则晶胞中所含硫酸根离子数目也为4,从晶胞示意图中可以发现有6个硫酸根离子,其中4个位于面上。故晶胞体内有2个硫酸根离子;以体心的亚铁离子为研究对象,每个硫酸根中均有一个氧原子离铁原子最近,亚铁离子周围最近的氧原子的个数为6;该晶胞的密度为: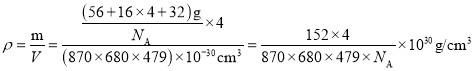 。答案为:2;2;6;
。答案为:2;2;6;![]() 。
。


科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CS(NH2)2 (硫脲)是一种白色晶体,139C时 溶解度为9.2g·(100gH2O)-1,可用于制造药物、染料等。由H2NCN(氰氨)与Na2S溶液等作原料,在约50°C、pH 10~11时制取,实验装置(夹持及加热装置已略)如下:
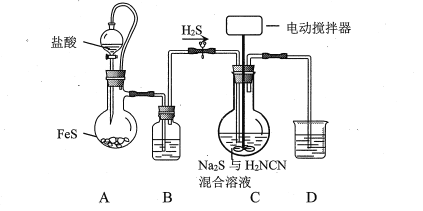
(1)装置B、D中盛放的试剂分别是__________、 _________。
(2)装置C合适的加热方式是___________。
(3)烧瓶中Na2S与等物质的量的H2NCN反应的化学方程式为_________________________________;以合适的流速通入H2S的目的是_________________________。
(4)实验过程中需分次加入H2NCN并继续通入H2S,经多次重复直至液体中出现絮状物。设计后续操作以从装置C的反应液中分离得到硫脲晶体的实验方案:______________________[实验中必须使用的试剂:NaOH溶液]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各有机物的数目与分子式C4H7ClO2且能与NaHCO3溶液反应生成CO2的有机物的数目(不考虑立体异构)相同的是
A.分子式为C5H10的烯烃B.甲苯的一氯代物
C.相对分子质量为74的一元醇D.立方烷(![]() )的二硝基取代物
)的二硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液为强电解质溶液,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空
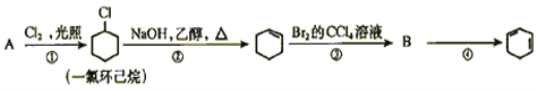
(1)A的名称是__________B的结构简式是_________
(2)②的反应类型是__________。③的反应类型是__________。
(3)反应④的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾和碘的相关化合物在化工医药材料等领域有广泛的应用。回答下列问题:
(1)基态K原子中,核外运动状态不同的电子共________种,占据最高能级的电子的电子云轮廓图形状为________。
(2)K和Cr属于同一周期,且核外最外层电子构型相同。第一电离能比较:K________(填“>”或“<”)Cr,金属键强度比较:K________(填“>”或“<")Cr.
(3)IO3-离子的立体构型的名称为________,中心原子的杂化方式为________.
(4)HIO4的酸性强于HIO3,其原因为________
(5)KIO3晶体是一种性能良好的非线性光学材料,晶胞如图。
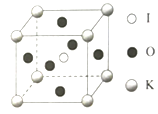
晶胞的棱长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,K与I间的最短距离为________nm,与K紧邻的O的个数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5 mL 0.005 mol·L-1的FeCl3溶液与5 mL0.01 mol·L-1的KSCN溶液混合,建立平衡:FeCl3+3KSCN![]() 3KCl+Fe(SCN)3(红色)。
3KCl+Fe(SCN)3(红色)。
(1)若滴加饱和FeCl3溶液4滴,平衡向________方向移动,溶液红色________。
(2)若滴加1 mol·L-1KSCN溶液4滴,平衡向________方向移动,溶液红色________。
(3)若滴加0.01 mol·L-1NaOH溶液4滴,则产生____ (填颜色)沉淀,c(Fe3+)___,平衡向______方向移动,溶液红色________。
(4)若加入少量KCl固体,则平衡________移动,原因________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com