
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10﹣9 | 6.8×10﹣6 | 5.5×10﹣6 | 1.8×10﹣11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为 不能 (填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是 贝壳研磨成粉末仍是CaCO3,由于CaCO3比MgCO3还要难溶,所以将其直接投入海水中不能产生MgCO3 ;如果不能直接投入,应将贝壳作何处理,试写出化学方程式 CaCO3\frac{\underline{\;高温\;}}{\;}CaO+CO2↑ .
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为 可以 (填“可以”或“不可以”)得到Mg(OH)2.在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他 能 (填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是 Mg2++CO32﹣=MgCO3 MgCO3+2OH﹣=Mg(OH)2+CO32﹣ .(用离子方程式表示)
(3)已知海水中镁离子浓度为1.8×10﹣3mol/L,则要使镁离子产生沉淀,溶液的pH最低应为 10 .
| 海水资源及其综合利用.. | |
| 分析: | (1)根据贝壳(主要成分是CaCO3)的溶解性分析;把CaCO3转化为CaO,CaO能与水反应生成碱; (2)模拟生产过程,烧碱也可以沉淀镁离子,若加入的是纯碱碳酸钠,会生成碳酸镁,加入氢氧化钠溶液,依据碳酸镁和氢氧化镁沉淀溶度积计算可知,氢氧化镁溶解度小于碳酸镁,可以实现沉淀转化生成氢氧化镁; (3)根据Ksp[Mg(OH)2]=c(Mg2+)×c2(OH﹣),结合已知离子浓度计算. |
| 解答: | 解:(1)已知贝壳(主要成分是CaCO3)的难溶于水,而且比MgCO3还要难溶,所以将CaCO3其直接投入海水中不能产生MgCO3;把CaCO3转化为CaO,其反应方程式为:CaCO3 故答案为:不能;贝壳研磨成粉末仍是CaCO3,由于CaCO3比MgCO3还要难溶,所以将其直接投入海水中不能产生MgCO3;CaCO3 (2)模拟该生产过程,但实验室无石灰,用烧碱也可以沉淀镁离子.Mg2++2OH﹣=Mg(OH)2↓,若加入的是纯碱碳酸钠,可以反应生成微溶于水的碳酸镁沉淀,到的混合体系中加入过量的烧碱溶液,氢氧化镁溶解度小于碳酸镁,实现沉淀转化生成氢氧化镁沉淀,过程中反应的离子方程式为:Mg2++CO32﹣=MgCO3,MgCO3+2OH﹣=Mg(OH)2+CO32﹣; 故答案为:可以,能,Mg2++CO32﹣=MgCO3 MgCO3+2OH﹣=Mg(OH)2+CO32﹣; (3)已知某地海水中的镁离子的浓度为1.8×10﹣3 mol•L﹣1,则c2(OH﹣)= 则c(H+)=1.0×10﹣10 mol•L﹣1,所以pH=10; 故答案为:10. |
| 点评: | 本题考查了溶度积常数的应用、守恒法在计算中的应用等,侧重考查学生分析问题的能力、解决问题的能力,题目难度中等. |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.钠与水反应:Na+2H2O===Na++2OH-+H2↑
B.硅酸钠溶液与醋酸溶液混合:SiO+2H+===H2SiO3↓
C.0.01 mol·L-1 NH4Al(SO4)2溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合:NH+
Al3++2SO+2Ba2++4OH-===2BaSO4↓+Al(OH)3↓+NH3·H2O
D.浓硝酸中加入过量铁粉并加热:Fe+3NO+6H+Fe3++3NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )

|
| A. | Z元素的原子半径可能比Y元素的小 |
|
| B. | W的原子序数可能是Y的原子序数的2倍 |
|
| C. | W的气态氢化物的稳定性一定比Y的强 |
|
| D. | Z的化学活泼性一定比X强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )
|
| A. | 漂白粉露置在空气中失效:ClO﹣+CO2+H2O=HClO+HCO3﹣ |
|
| B. | 向NaAlO2溶液中通入过量CO2:AlO2﹣+CO2+2H2O=Al(OH)3↓+HCO3﹣ |
|
| C. | 向Na2S2O3溶液中通入足量氯气:S2O32﹣+2Cl2+3H2O=2SO32﹣+4Cl﹣+6H+ |
|
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+Fe(OH)3=FeO42﹣+3Cl﹣+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
双隔膜电解池的结构示意简图如图所示,对该装置及其原理判断错误的是
( )
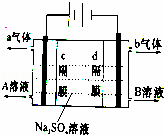
|
| A. | c隔膜为阴离子交换膜、d隔膜为阳离子交换膜 |
|
| B. | A溶液为硫酸,B溶液为氢氧化钠 |
|
| C. | a气体为氢气,b气体为氧气 |
|
| D. | 该电解反应的总方程式为:2Na2SO4+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在指定条件下电离方程式正确的是 ( )
A.Na2CO3溶于水 Na2CO3===Na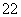 +CO
+CO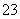
B.Al(OH)3酸式电离 Al(OH)3===H++AlO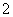 +H2O
+H2O
C.NaHS溶于水HS-的电离 HS-+H2O H2S+OH-
H2S+OH-
D.NaHCO3加热熔化 NaHCO3===Na++HCO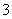
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是 ( )
A.硫酸铝溶液中加入过量氨水:Al3++3OH-===Al(OH)3 ↓
B.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO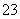 ===CaCO3↓+2OH-
===CaCO3↓+2OH-
C.冷的氢氧化钠溶液中通入氯气:Cl2+2OH-===ClO-+Cl-+ H2O
D.稀硫酸中加入铁粉:2Fe+6H+===2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
NaClO2可用作造纸的漂白剂,它由H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2制得,下列说法正确的是
A.H2O2是氧化剂,H2O2中的氧元素被还原
B.每生成1 mol O2转移的电子的物质的量为4 mol
C.ClO2中的氯元素被氧化
D.ClO2是氧化剂,H2O2是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com