
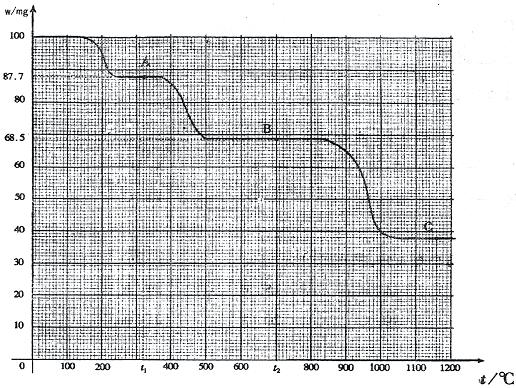
下图是100 mg CaC2O4·H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识填空:
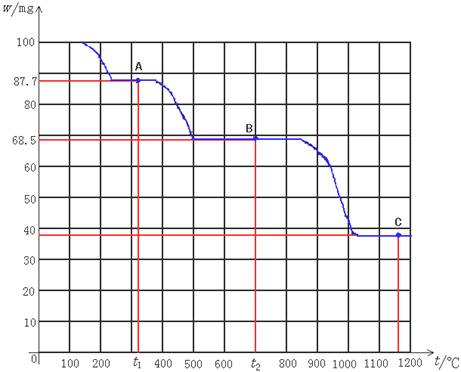
(1)温度分别为t1和t2时,固体产物的化学式A是________,B是________。产物C的化学式为 。
(2)由A得到B的化学方程式为___________________________________。
(1)CaC2O4
CaCO3 CaO (均1分,共3分)(2)CaC2O4 CaCO3+CO↑ (2分)
CaCO3+CO↑ (2分)
【解析】根据题目要求可分3段讨论CaC2O4•H2O的受热分解.
(1)t1时A点,100mgCaC2O4•H2O的质量减少至87.7mg,从中分析CaC2O4•H2O受热分解的产物,固体CaC2O4•H2O的摩尔质量为146g/mol,设分解后产物的摩尔质量为M1.100×10-3g÷146g/mo=87.7×10-3g÷M1,解得M1=128.04g/mol。由于CaC2O4的摩尔质量为128g/mol,从而判断出CaC2O4•H2O的分解反应方程式为:CaC2O4•H2O  CaC2O4+H2O↑
CaC2O4+H2O↑
所以A的化学式是CaC2O4.
(2)再讨论t2时B点,87.7mg的CaC2O4受热分解,设分解产物的摩尔质量为M2.
则87.7×10-3g÷28g/mol=68.5×10-3g÷M2.解得M2=99.98g/mol。从M2的实验值可推断出产物B应为CaCO3,分解方程式为:CaC2O4 CaCO3+CO↑
CaCO3+CO↑
(3)综上分析,由CaC2O4•H2O得到A的化学方程式即为CaC2O4 CaCO3+CO↑
CaCO3+CO↑
(4)当加热至1100℃~1200℃时,由图读得分解产物C的质量约为38mg,设C点化合物摩尔质量为M3.则68.5×10-3g÷100g/mol=38×10-3g÷M3.解得M3=55.47g/mol。M3的实验值与CaO的摩尔质量(56g/mol)接近,分解方程式应为:CaCO3 CaO+CO2↑。由此得出C的化学式为CaO,其分子量即为56.
CaO+CO2↑。由此得出C的化学式为CaO,其分子量即为56.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
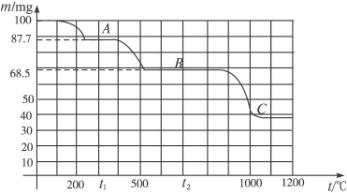
(1)温度分别为t1和t2时,固体产物的化学式A是______________,B是______________。
(2)由CaC2O4·H2O得到A的化学方程式为__________________________________。
(3)由A得到B的化学方程式为____________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:
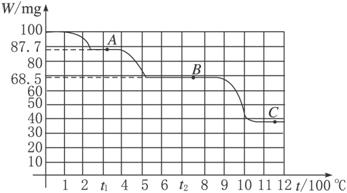
(1)温度分别为t1和t2时,固体产物的化学式A是______________,B是________________。
(2)由CaC2O4·H2O得到A的化学方程式为_______________________________________。
(3)由A得到B的化学方程式为___________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省余姚中学高一下学期期中考试实验班化学试卷(带解析) 题型:计算题
下图是100 mg CaC2O4·H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识填空: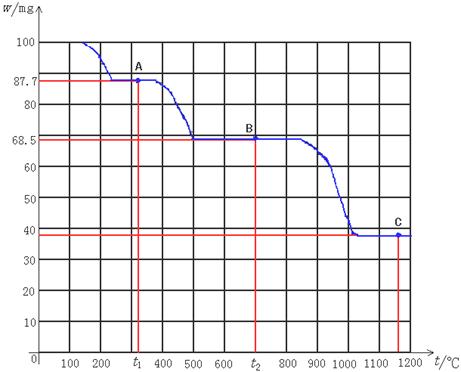
(1)温度分别为t1和t2时,固体产物的化学式A是________,B是________。产物C的化学式为 。
(2)由A得到B的化学方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)温度分别为t1和t2时,固体产物的化学式A是 ,B是 。
(2)由CaC2O4·H2O得到A的化学方程式为 。
(3)由A得到B的化学方程式为 。
(4)由图计算产物C的分子量,并推断C的合理的化学式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com