
下列实验操作错误的是( )。
A.用钥匙取用少量的Na2SO4固体
B.用胶头滴管滴加少量的NaCl溶液
C.加热盛有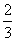 体积K2SO4溶液的试管
体积K2SO4溶液的试管
D.用10mL的量筒量取8mL1.0mol/LNaOH溶液
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1 mol氢气中的化学键需要吸收436 kJ能量;破坏1/2 mol氧气中的化学键需要吸收 249 kJ的能量;形成水分子中1 mol H—O键能够释放 463 kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上。
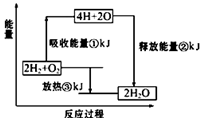
①________kJ ②________kJ ③________kJ
(2)今有2H2+O2 =2H2O反应构成燃料电池,则负极通的应是 ,用KOH溶液作电解质,负极的电极反应式为 ,正极的电极反应式为 。
(3)若把H2改为CH3OH,用KOH溶液作电解质,则负极的电极反应式: .
(4)电解原理在化学工业中有广泛的应用。右图表示一个电解池,电极材料为惰性电极,U形管装有饱和食盐水;实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中阴极上的电极反应式为______________________,在阴极附近观察到的现象是_______________。

②随着气体的生成,饱和食盐水中产生了两种不同的颜色:
阳极区是 色,阴极区是 色。
③电解一段时间后取出电极,将U形管内的液体搅拌混匀,又发生了化学反应,该反应的化学方程式是 ;该溶液可用作消毒剂,原因是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2===A+NH3↑,则生成物A的化学式为________,H2O2被称为“绿色氧化剂”的理由是________________________。
(3)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数约为____________。
(4)“84”消毒液(主要成分是NaClO)和洁厕 剂(主要成分是浓盐酸)不能混用,原因是__________
剂(主要成分是浓盐酸)不能混用,原因是__________ ________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的总反应为:
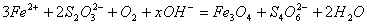 。下列说法正确的是( )。
。下列说法正确的是( )。
A.Fe2+、S2O32-都是还原剂 B.每生成1 mol Fe3O4,则转移电子数为3 mol
C.硫元素被氧化,铁元素被还原 D. x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,根据表中10种元素,用元素符号或化学式填空。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑨ | ⑧ | ⑩ |
(1)①~⑩元素中,金属性最强的是 ;化学性质最不活泼的是 。
(2)①~⑩元素中,最高价氧化物水化物呈两性的是 ,该化合物与NaOH溶液反应的离子方程式为 ;
(3)①~⑩元素中,最高价氧化物水化物酸性最强的是 ,碱性最强的是 ;
(4)⑤、⑥、⑧、⑨所形成的离子,其半径由小到大的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既是氧化还原反应,又是吸热反应的是( )。
A.铝片与稀H2SO4的反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应 D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是( )。
A.电池工作时,溶液中负极附近溶液的碱性增强,而电解质溶液pH减小
B.正极的电极反应式是:O2+4H++4e-=2H2O
C.负极的电极反应式是:N2H4+4OH――4e-=4H2O+N2↑ D.溶液中阴离子向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH— 2CO32— + 6H2O,则下列说法错误的是 ( )
A.放电时CH3OH参与反应的电极为正极 B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32— + 6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com