
【题目】N元素的单质及其化合物之间的转化关系:NH3N2NO NO2HNO3。回答下列问题:
(1)N元素在元素周期表中的位置为_______;
(2)上述四种气体只能用排水法收集的是_______(填化学式,下同),只能用排空气法收集的是______;
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_____;
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为______;
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程______;
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度_______(写出解题过程)。
【答案】第二周期,第VA族 NO、N2 NH3、NO2 ABD 3NO2+H2O=2HNO3+NO 2NO+2CO![]() 2CO2+N2 13 mol/L
2CO2+N2 13 mol/L
【解析】
(5)在催化剂存在下可将NO和CO反应转化为两种无色无毒气体是N2、CO2,根据电子守恒及原子守恒,书写反应方程式;
(6)先计算Cu及气体的物质的量,根据HNO3反应后变为Cu(NO3)2、NO、NO2,利用N元素守恒计算硝酸的物质的量,最后根据物质的量浓度定义式计算硝酸的浓度。
(1)N是7号元素,原子核外电子排布是2、5,因此在周期表的位置是位于第二周期第VA族;
(2)在上述四种气体中NO能够与空气中的O2反应产生NO2,因此只能使用排水法收集;N2的相对分子质量是28,与空气的平均相对分子质量29,二者非常接近,若采用排空气方法收集,不能得到纯净气体,因此只能采用排水方法收集;
NH3极容易溶于水,并且与水会发生反应产生NH3·H2O,结合其密度比空气小的特点,NH3只能采用向下排空气方法收集;NO2与H2O反应产生HNO3、NO,因此也不能采用排水方法收集,由于其相对分子质量比空气大,要采用向上排空气方法收集;
(3)A. 酸雨是由SO2及氮的氧化物等引起的,与氮的氧化物排放有关,A符合题意;
B. 光化学烟雾的形成主要是汽车尾气排放出的NO、NO2发生复杂变化造成的,与氮的氧化物排放有关,B符合题意;
C. 白色污染是塑料等造成的,与氮的氧化物排放无关,C不符合题意;
D. 臭氧层空洞与飞机尾气排放的NO、NO2及冰箱制冷剂氟利昂的排放有关,因此与氮的氧化物排放有关,D符合题意;
故合理选项是ABD;
(4)NO2与H2O反应产生HNO3、NO,反应方程式为:3NO2+H2O=2HNO3+NO,HNO3进入雨水中形成酸雨;
(5)在催化剂存在下,NO和CO反应转化为两种无色无毒气体是N2、CO2,根据电子守恒及原子守恒,可得反应方程式为:2NO+2CO![]() 2CO2+N2;
2CO2+N2;
(6)12.8 g铜的物质的量n(Cu)=![]() =0.2 mol,反应产生的标准状况下NO、NO2气体的物质的量n(NO+NO2)=
=0.2 mol,反应产生的标准状况下NO、NO2气体的物质的量n(NO+NO2)=![]() =0.25 mol,HNO3在反应中的作用:一部分转化为Cu(NO3)2,一部分变为NO、NO2气体,根据N元素守恒,可知HNO3的物质的量n(HNO3)=2[Cu(NO3)2]+ n(NO+NO2)=2×0.2 mol+0.25 mol=0.65 mol,由于硝酸的体积是50 mL,则该硝酸的物质的量浓度c(HNO3)=
=0.25 mol,HNO3在反应中的作用:一部分转化为Cu(NO3)2,一部分变为NO、NO2气体,根据N元素守恒,可知HNO3的物质的量n(HNO3)=2[Cu(NO3)2]+ n(NO+NO2)=2×0.2 mol+0.25 mol=0.65 mol,由于硝酸的体积是50 mL,则该硝酸的物质的量浓度c(HNO3)=![]() =13 mol/L。
=13 mol/L。


科目:高中化学 来源: 题型:
【题目】我国科学家开发设计一种天然气脱硫装置,利用如右图装置可实现:H2S+O2→H2O2 +S。已知甲池中有如下的转化:


下列说法错误的是:
A. 该装置可将光能转化为电能和化学能
B. 该装置工作时,溶液中的H+从甲池经过全氟磺酸膜进入乙池
C. 甲池碳棒上发生电极反应:AQ+2H+ +2e- =H2AQ
D. 乙池①处发生反应:H2S+I3- =3I-+S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种有机化合物,分子式都是C9H11O2N。
(1)化合物A是天然蛋白质的水解产物,光谱测定显示,分子结构中不存在甲基(—CH3)。化合物A的结构简式是____。
(2)化合物B是某种芳香烃与混酸在加热条件下进行硝化反应后的唯一产物。化合物B的结构简式是____。
(3)化合物C能发生银镜反应、水解反应,且 氢核磁共振谱显示只有4组峰。化合物C的结构简式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,近年来发现了一种新的星际分子,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、三键等,颜色相同的球表示同一种原子)。
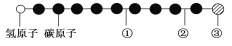
下列对该物质的说法中正确的是
A. ①处的化学键表示碳碳双键 B. ②处的化学键表示碳碳单键
C. ③处的原子可能是氯原子或氟原子 D. 此星际分子属于烃类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Mg、Al、Fe四种金属中两种组成的混合物12g,与足量盐酸反应放出H2 0.5 g(标准状况),则混合物中必定含有的金属是
A.钠B.镁C.铝D.铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(Ti)被誉为“21世纪的金属”,工业上将TiO2与焦炭混合,通入Cl2高温下制得TiCl4;再将TiCl4提纯后,在氩气保护下与镁高温反应制得Ti。其反应如下:
①TiO2+2Cl2+2C![]() TiCl4+2CO
TiCl4+2CO
②TiCl4+2Mg ![]() Ti+2MgCl2
Ti+2MgCl2
回答下列问题:
(1)Ti元素原子的价电子排布式为____________________;
(2)写出与CO互为等电子体的分子_________________;
(3)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体.
①TiCl4为______化合物(填“离子”或“共价”);
②TiCl4分子为正四面体形,则Ti为___________杂化.
③TiCl4在潮湿空气中水解的化学方程式是____________________;
④TiCl2、Cl2和C反应制得的TiCl4最好的提纯方法是__________(填操作名称)。
(4)配离子[TiCl(H2O)5]2+的中心离子化合价为_______,中心离子配位数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W 一种核素的质量数为 18,中子数为 10;X 和 Ne 的核外电子数相差1;在Z所在的周期中,Z元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:
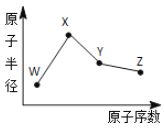
(1)X元素位于元素周期表中位置为_____________。
(2)X的单质和 Y 的单质相比,熔点较高的是____________(写化学式) 。Z所在族的简单氢化物中,沸点最高的是________(写化学式),原因为______________________。
(3)W、X、Z三种元素形成的化合物中化学键类型为_______;X2W2的电子式为_______。
(4)Z的氧化物很多,其中一种黄绿色气体 M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性 。 M 的化学式为___________。M可与NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半水煤气是工业合成氨的原料气,其主要成分为H2、CO、CO2、N2和H2O(g)。半水煤气经过下列步骤转化为合成氨的原料。
![]()
(1)步骤I,CO变换反应的能量变化如下图所示:

①CO变换反应的热化学方程式是________________。
②一定条件下,向体积固定的密闭容器中充入aL半水煤气,发生CO变换反应。测得不同温度(T1,T2)氢气的体积分数ψ(H2)与时间的关系如下所示。
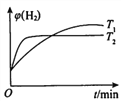
i.T1、T2的大小关系及判断理由是______________。
ii.请在上图中画出:其他条件相同时,起始充入0.5aL半水煤气,T2温度下氢气的体积分数ψ( H2)随时间的变化曲线。______________
(2)步骤Ⅱ,用饱和Na2CO3溶液作吸收剂脱除CO2时,初期无明显现象,后期有固体析出。
①溶液中离子浓度关系正确的是__________(选填字母)。
a.吸收前:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)
b.吸收初期:2c(CO32-)+2 c(HCO3-)+2c(H2CO3)=c(Na+)
c.吸收全进程:c(Na+)+c( H+)=2c(CO32-)+ c(HCO3-)+ c(OH-)
②后期析出固体的成分及析出固体的原因是___________。
③当吸收剂失效时,请写出一种可使其再生的方法(用化学方程式表示):____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种食品保鲜剂,可按如下途径合成:
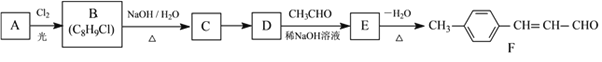 已知:RCHO+CH3CHO
已知:RCHO+CH3CHO![]() RCH(OH)CH2CHO。
RCH(OH)CH2CHO。
试回答:
(1)A的化学名称是____,A→B的反应类型是____。
(2)B→C反应的化学方程式为________。
(3)C→D所用试剂和反应条件分别是_____。
(4)E的结构简式是_____。F中官能团的名称是_____。
(5)连在双键碳上的羟基不稳定,会转化为羰基,则D的同分异构体中,只有一个环的芳香族化合物有____种。
其中苯环上只有一个取代基,核磁共振氢谱有5个峰,峰面积比为2∶1∶2∶2∶1的同分异构体的结构简式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com