
将Fe粉、Cu粉、FeCl3溶液、FeCl2溶液和CuCl2溶液,混合于某容器中充分反应(假定容器不参与反应),试判断下列情况下溶液中存在的金属离子和金属单质.
(1)若铁粉有剩余,则容器中不可能有________.
(2)若氯化铜有剩余,则容器中还可能有________.
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有________,可能有________.
(4)若氯化铁有剩余,则容器中不可能有________.
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
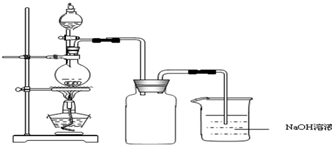 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Fe(OH)2 | 开始沉淀pH | 2.7 | 4.8 | 7.6 | 完全沉淀pH | 3.7 | 6.4 | 9.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com