
¹¤ŅµÉĻŅ»°ćŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ²ÉÓĆĻĀĮŠ·“Ó¦ŗĻ³É¼×“¼£ŗ
CO(g)£«2H2(g)  CH3OH(g)””¦¤H
CH3OH(g)””¦¤H
(1)ÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ(Ģī×ÖÄøŠņŗÅ£¬ĻĀĶ¬)________”£
A£®Éś³ÉCH3OHµÄĖŁĀŹÓėĻūŗÄCOµÄĖŁĀŹĻąµČ
B£®»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä
C£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä
D£®CH3OH”¢CO”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ
(2)ĻĀ±ķĖłĮŠŹż¾ŻŹĒ·“Ó¦ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»ÆŃ§Ę½ŗā³£Źż(K)”£
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
¢ŁÓɱķÖŠŹż¾ŻÅŠ¶Ļ¦¤H________(Ģī”°>”±”¢”°£½”±»ņ”°<”±)0£»
¢ŚÄ³ĪĀ¶ČĻĀ£¬½«2 mol COŗĶ6 mol H2³äČė2 LµÄĆܱÕČŻĘ÷ÖŠ£¬³ä·Ö·“Ó¦ŗ󣬓ļµ½Ę½ŗāŹ±²āµĆc(CO)£½0.2 mol/L£¬ŌņCOµÄ×Ŗ»ÆĀŹĪŖ________£¬“ĖŹ±µÄĪĀ¶ČĪŖ________”£
(3)ŅŖĢįøßCOµÄ×Ŗ»ÆĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ________”£
A£®ÉżĪĀ”””””””””””””” B£®¼ÓČė“߻ƼĮ C£®Ōö¼ÓCOµÄÅØ¶Č D£®¼ÓČėH2¼ÓŃ¹ E£®¼ÓČė¶čŠŌĘųĢå¼ÓŃ¹ F£®·ÖĄė³ö¼×“¼
(4)300”ꏱ£¬ŌŚŅ»¶ØµÄŃ¹ĒæĻĀ£¬5 mol COÓė×ćĮæµÄH2ŌŚ“߻ƼĮµÄ×÷ÓĆĻĀĒ”ŗĆĶźČ«·“Ó¦±ä»ÆµÄČČĮæĪŖ454 kJ”£ŌŚøĆĪĀ¶ČŹ±£¬ŌŚČŻ»żĻąĶ¬µÄ3øöĆܱÕČŻĘ÷ÖŠ£¬°“²»Ķ¬·½Ź½Ķ¶Čė·“Ó¦Īļ£¬±£³ÖŗćĪĀ”¢ŗćČŻ£¬²āµĆ·“Ó¦“ļµ½Ę½ŗāŹ±µÄÓŠ¹ŲŹż¾ŻČēĻĀ£ŗ
| ČŻĘ÷ | ¼× | ŅŅ | ±ū | |
| ·“Ó¦ĪļĶ¶ČėĮæ | 1 mol CO”¢2 mol H2 | 1 mo l CH3OH | 2 mol CH3OH | |
| Ę½ŗāŹ±Źż¾Ż | CH3OHµÄ ÅضČ(mol/L) | c1 | c2 | c3 |
| ·“Ó¦µÄÄÜ | ||||
| Įæ±ä»Æ | a kJ | b kJ | c kJ | |
| ĢåĻµŃ¹Ēæ(Pa) | p1 | p2 | p3 | |
| ·“Ó¦Īļ×Ŗ»ÆĀŹ | ¦Į1 | ¦Į2 | ¦Į3 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ________”£
A£®2c1>c3 B£®a£«b<90.8 C£®2p2<p3 D£®¦Į1£«¦Į3<1

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĪļÖŹÖŠ£¬°“Äܵ¼µē”¢ŹĒĒæµē½āÖŹ”¢ŹĒČõµē½āÖŹ”¢ŹĒ·Ēµē½āÖŹµÄĖ³ŠņÅÅĮŠµÄŹĒ (””””)
A.Cu””CaCO3””±ł“×Ėį””SO2
B.CuSO4¾§Ģå””NaOH””NH3”¤H2O””CH3CH2OH
C.ŹÆÄ«””NaCl””H3PO4””Cu
D.ČŪČŚNaCl””Na2O””AlCl3””CCl4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪŖĮĖ³żČ„CO2ĘųĢåÖŠµÄSO2ĘųĢ壬ĻĀĮŠ¶ŌÓŚŅĒĘ÷ŗĶŅ©Ę·µÄ×éŗĻÖŠŗĻĄķµÄŹĒ£Ø £©”£
ŅĒĘ÷£ŗ¢ŁĻ“ĘųĘæ ¢ŚøÉŌļ¹Ü
Ņ©Ę·£ŗ¢ŪÉśŹÆ»Ņ ¢ÜĖÕ“ņČÜŅŗ ¢ŻŠ”ĖÕ“ņČÜŅŗ
A£®¢Ł¢Ż B£®¢Ś¢Ż C£®¢Ł¢Ū D£®¢Ł¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ±ķŹ¾¶ŌÓ¦»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A. µē½ā±„ŗĶMgCl2ČÜŅŗ£ŗ2Cl££«2H2O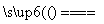 2OH££«H2”ü£«Cl2”ü
2OH££«H2”ü£«Cl2”ü
B£®ĻņNa2SO3ČÜŅŗÖŠµĪ¼Ó×ćĮæNaClOČÜŅŗ£ŗSO + ClO£= SO
+ ClO£= SO + Cl£
+ Cl£
C£®ĻņFeBr2ČÜŅŗÖŠĶØČė×ćĮæCl2£ŗ2Fe2++Cl2=2Fe3++2Cl£
D£®ĻņCa(OH)2ČÜŅŗÖŠ¼ÓÉŁĮæNaHCO3ČÜŅŗ£ŗ
2 HCO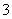 +Ca2++2OH£=CaCO3”ż+ CO
+Ca2++2OH£=CaCO3”ż+ CO +2H2O
+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠøł¾ŻŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆ³öµÄ½įĀŪ“ķĪóµÄŹĒ
| Ń”Ļī | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| A | ĻņAgCl³ĮµķÖŠµĪ¼ÓÉŁĮæKIČÜŅŗ | ³Įµķ±äĪŖ»ĘÉ« | Ksp(AgCl)> Ksp(AgI) |
| B | ĻņČÜŅŗXÖŠ¼ÓČėŃĪĖįĖį»ÆµÄBaCl2ČÜŅŗ | ³öĻÖ°×É«³Įµķ | ČÜŅŗÖŠŅ»¶Øŗ¬ÓŠSO |
| C | ŌŚ0.1mol”¤L£1 Na2CO3ČÜŅŗÖŠ£¬¼ÓĮ½µĪ·ÓĢŖĻŌĒ³ŗģÉ«£¬Ī¢ČČ | ŗģÉ«¼ÓÉī | øĆĖ®½āŹĒĪüČČ·“Ó¦ |
| D | ĻņČÜŅŗYÖŠ¼ÓČėĻ”ŃĪĖį£¬²¢½«²śÉśµÄĪŽÉ«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ® | ÓŠ°×É«³ĮµķÉś³É | ČÜŅŗÖŠæÉÄÜŗ¬ÓŠCO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķź³ÉĻĀĮŠŹµŃéĖłŠčŃ”ŌńµÄ×°ÖĆ»ņŅĒĘ÷¶¼ÕżČ·µÄŹĒ
(””””)
| A | B | C | D | |
| ŹµŃé | ·ÖĄėÖ²ĪļÓĶŗĶĀČ»ÆÄĘČÜŅŗ | ³żČ„ĀČ»ÆÄĘ¾§ĢåÖŠ»ģÓŠµÄĀČ»Æļ§¾§Ģå | ·ÖĄėCCl4ÖŠµÄBr2 | ³żČ„CO2ĘųĢåÖŠµÄHClĘųĢå |
| ×°ÖĆ »ņŅĒĘ÷ |
|
|
|
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A£®øɱł”¢ŅŗĢ¬ĀČ»ÆĒā¶¼ŹĒµē½āÖŹ
B£®Na2O2¾§ĢåÖŠ¼Čŗ¬ÓŠĄė×Ó¼üÓÖŗ¬ÓŠ¹²¼Ū¼ü
C£®Na2O”¢Fe2O3”¢Al2O3¼ČŹōÓŚ¼īŠŌŃõ»ÆĪļ£¬ÓÖŹōÓŚĄė×Ó»ÆŗĻĪļ
D£®øł¾ŻŹĒ·ń¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬½«·ÖÉ¢Ļµ·ÖĪŖČÜŅŗ”¢×ĒŅŗŗĶ½ŗĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«4.6 g CuŗĶMgĶźČ«ČÜÓŚÅØĻõĖįČÜŅŗÖŠ£¬·“Ó¦ÖŠĻõĖįµÄ»¹Ō²śĪļĪŖ4480mL NO2ĘųŗĶ336 mL N2O4ĘųĢå(±ź×¼×“æöĻĀ)£¬·“Ó¦ŗóµÄČÜŅŗÖŠ£¬¼ÓČė¹żĮæNaOHČÜŅŗ£¬Éś³É³ĮµķµÄÖŹĮæĪŖ ( )
A£®9.02 g B£®8.51 g C£®8.26 g D£®7.04 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ć¾”¢ĀĮÄܹ»ŌŚæÕĘųÖŠĪČ¶Ø“ęŌŚµÄŌŅņŹĒ£Ø £©”£
A£®ŠŌÖŹ²»»īĘĆ£¬²»ÓėæÕĘųÖŠµÄ³É·Ö·“Ó¦
B£®Ć¾”¢ĀĮÓėŃõĘųµÄ·“Ó¦ĖŁĀŹ¼«Āż
C£®¾¹żĮĖĢŲŹā¹¤ŅÕ“¦Ąķ
D£®ÓėŃõĘų·“Ó¦ŠĪ³ÉĮĖŃõ»ÆĪļ±£»¤Ä¤
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com