
| A. | 白磷 | B. | 石英 | C. | 烧碱 | D. | 食盐 |
分析 (1)共价键是原子间通过共用电子对形成的强的相互作用;
(2)离子键是通过阴阳离子间的静电作用形成的;
(3)分子间作用力是分子之间的相互作用,不是化学键,作用力弱;
(4)一种物质中可以同时存在离子键、共价键,分子间作用力只存在于分子间.
解答 解:A、白磷为分子晶体,存在分子间作用力,同时存在P-P共价键,故A正确;
B、石英的主要成分是SiO2,它是由原子构成的物质,原子间通过共价键形成空间网状结构,只存在共价键,故B错误;
C、烧碱是离子化合物,由钠离子和氢氧根离子构成,阴阳离子间形成的是离子键,氢原子和氧原子以共价键形成氢氧根离子,故C正确;
D、食盐是离子化合物,由钠离子和氯离子构成,只存在离子键,故D错误;
故选AC.
点评 本题考查了分子晶体、原子晶体、离子晶体等几种典型物质的结构,重点考查构成物质微粒之间的相互作用,化学键的形成实质是相邻原子间强的相互作用,分子间作用力是分子间弱的作用不属于化学键.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{A}$(m+N)mol | B. | $\frac{a}{A+2m}$ (A-N+m)mol | C. | $\frac{a}{A+m}$(A-N+m)mol | D. | $\frac{a}{A+2m}$(m+N)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用浓硝酸洗去银镜 | |
| B. | 向2%的稀氨水中滴入2%的硝酸银溶液,配得银氨溶液 | |
| C. | 采用水浴加热,也可以直接加热 | |
| D. | 试管先用热NaCl溶液洗涤,然后用蒸馏水洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
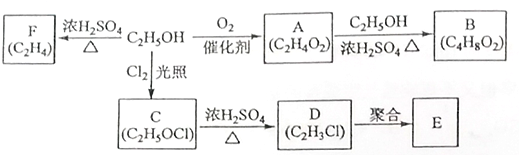
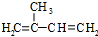 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$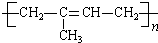 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的酸性强于硫化氢 | |
| B. | 氯化氢的稳定性比硫化氢强 | |
| C. | 氯气能与水反应而硫不能 | |
| D. | 氯原子最外电子层上有7个电子而硫最外电子层上有6个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
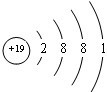 .
.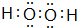 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3体积/mL | 26.90 | 26.55 | 27.00 | 26.95 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com