
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | 说明Y中不含醛基 |
| C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(已转化为标准状况下) | 测定铝箔中氧化铝的含量 |
| D | 比较不同反应的反应热数据大小 | 从而判断反应速率的大小 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硝酸根离子在酸性条件下具有强氧化性,也可氧化亚铁离子;
B.醛基与氢氧化铜的反应应在碱性条件下进行;
C.根据氢气的体积可确定铝的量;
D.反应热与反应速率没有必要联系.
解答 解:A.不能排除硝酸根离子的影响,应在硫酸铁溶液中加入硫酸酸化的过氧化氢,故A错误;
B.向1mL 1%的NaOH溶液中加入2mL 2%的CuSO4溶液,碱不足,醛基与氢氧化铜的反应应在碱性条件下进行,故B错误;
C.铝和氢氧化钠发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据氢气的体积可确定铝的量,可用测定含量,故C正确;
D.反应热与反应速率没有必要联系,故D错误.
故选C.
点评 本题考查化学实验方案的评价,涉及物质的检验、反应速率的影响等知识,侧重于学生的分析能力、实验能力和评价能力的考查,为高考常见题型和高频考点,注意把握实验的严密性和合理性,难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 解释 |
| A | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 | Cl2和SO2均具有漂白性 |
| B | Fe与稀硝酸、稀硫酸反应均有气泡产生 | Fe与两种酸均发生置换反应 |
| C | 某物质燃烧后的产物既能使白色硫酸铜粉末变蓝,又能使澄清石灰水变浑浊 | 该物质可能是碳氢化合物 |
| D | 向某有机物的水溶液中加Na产生大量气体 | 该有机物中可能含有羟基或羧基 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
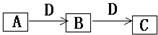 A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化如图所示(部分产物已略去).
A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化如图所示(部分产物已略去).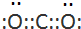 ,及A与C反应的离子方程式:OH-+HCO3-=CO32-+H20;
,及A与C反应的离子方程式:OH-+HCO3-=CO32-+H20;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向苯酚钠溶液通入少量的CO2:2O-+CO2+H2O-→2OH+CO32- | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO3-═Ag++NO↑+2H2O | |
| C. | (NH4)2Fe(SO4)2溶液与过量Ba(OH)2溶液混合:Fe2++2SO42-+2Ba2++2OH-═Fe(OH)2↓+2BaSO4↓ | |
| D. | 常温下,向澄清石灰水中通入Cl2:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
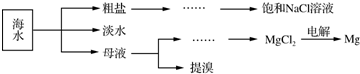
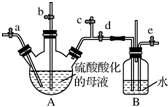
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
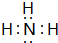 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
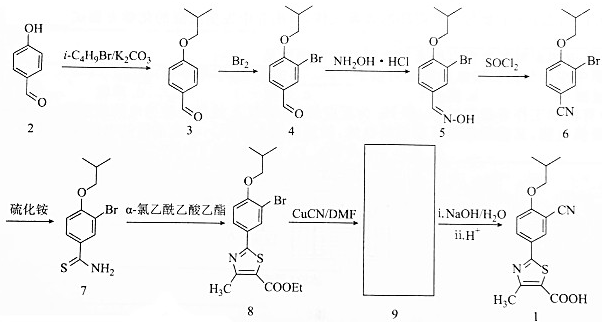
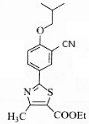 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据焓和熵的观点,石墨比金刚石稳定 | |
| B. | 根据焓和熵的观点,金刚石比石墨隐定 | |
| C. | 根据熵的观点,石墨比金刚石稳定,但根据焓的观点,金刚石比石墨稳定 | |
| D. | 根据焓的观点,石墨比金刚石稳定,但根据熵的观点,金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核外电子有六种运动状态 | |
| B. | L能层p能级只有一个空轨道 | |
| C. | L能层有两个未成对的电子 | |
| D. | 最外层p能级电子数与次外层电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com